(15分)资源化利用CO2不仅可以减少温室气体的排放,还可以重新获得燃料或重要工业产品。
(1)有科学家提出可利用FeO吸收和利用CO2,相关热化学方程式为:6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △H=-76.0kJ/mol,该反应中每生成1mol Fe3O4,转移电子的数目为。
(2)在一定条件下,二氧化碳转化为甲烷的反应为:CO2(g)+4H2(g)  CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
①向一容积为2L的恒容密闭容器中充入一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2 0.2mol/L, H2 0.8 mol/L, CH4 0.8 mol/L, H2O 1.6 mol/L。起始充入CO2和H2的物质的量分别为、。CO2的平衡转化率为。
②现有两个相同的恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ,在Ⅰ中充入1mol CO2和4molH2,在Ⅱ中充入1mol CH4和2molH2O(g),300℃开始反应,达到平衡时,下列说法正确的是()(填字母)。
| A.容器Ⅰ、Ⅱ中正反应速率相同 |
| B.容器Ⅰ、Ⅱ中反应的平衡常数相同 |
| C.容器Ⅰ中CO2的物质的量比容器Ⅱ中的多 |
| D.容器Ⅰ中CO2的转化率与容器Ⅱ中CH4的转化率之和小于1 |
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如下图所示:
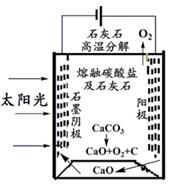
①上述生产过程的能量转化方式是、。
②上述电解反应在温度小于900℃时进行,碳酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极电极反应式为,阴极电极反应式为。
 ,且均为链状结构。(已知有机物中同一个碳上连接两个羟基不稳定)
,且均为链状结构。(已知有机物中同一个碳上连接两个羟基不稳定)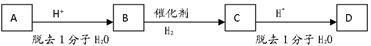
 _________________
_________________

 CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
 H++SO42-。.
H++SO42-。. 粤公网安备 44130202000953号
粤公网安备 44130202000953号