如图,已知:①单质E可作为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈酸性,它能够跟氧化物A起反应.据此,请填空: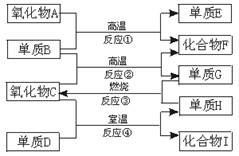
(1)化合物F是__________。(2)化合物I是__________。
(3)反应③的化学方程式是__________。(4)反应④的化学方程式__________。
如图,已知:①单质E可作为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈酸性,它能够跟氧化物A起反应.据此,请填空:
(1)化合物F是__________。(2)化合物I是__________。
(3)反应③的化学方程式是__________。(4)反应④的化学方程式__________。