萜品醇可作为消毒剂、抗氧化剂、医药和溶剂。合成a-萜品醇G的路线之一如下:
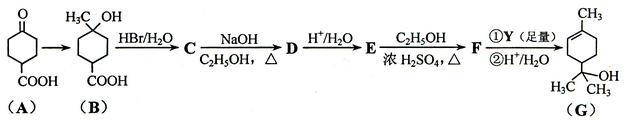
已知:
请回答下列问题:
⑴ 所含官能团的名称是
⑵ 催化氢化得,写出在一定条件下聚合反应的化学方程式:
⑶ 的分子式为
① 核磁共振氢谱有2个吸收峰 ② 能发生银镜反应
(4) 、的反应类型分别为
⑸ 的化学方程式为
⑹ 试剂的结构简式为
⑺ 通过常温下的反应,区别、和的试剂是
⑻ 与催化加成得不含手性碳原子(连有4个不同原子或原子团的碳原子叫手性碳原子)的化合物,写出的结构简式:
萜品醇可作为消毒剂、抗氧化剂、医药和溶剂。合成a-萜品醇G的路线之一如下:
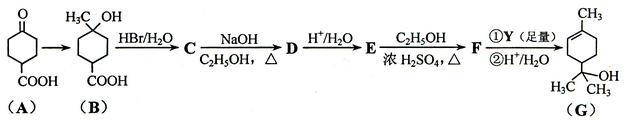
已知:
请回答下列问题:
⑴ 所含官能团的名称是
⑵ 催化氢化得,写出在一定条件下聚合反应的化学方程式:
⑶ 的分子式为
① 核磁共振氢谱有2个吸收峰 ② 能发生银镜反应
(4) 、的反应类型分别为
⑸ 的化学方程式为
⑹ 试剂的结构简式为
⑺ 通过常温下的反应,区别、和的试剂是
⑻ 与催化加成得不含手性碳原子(连有4个不同原子或原子团的碳原子叫手性碳原子)的化合物,写出的结构简式: