[江西]2011-2012学年江西省南昌市四校高二第二次联考化学试卷
某反应的△H=+100k J·mol-1,下列有关该反应的叙述正确的是
J·mol-1,下列有关该反应的叙述正确的是
| A.正反应活化能小于100kJ·mol-1 | B.逆反应活化能一定小于100kJ·mol-1 |
| C.逆反应活化能不小于100kJ·mol-1 | D.正反应活化能比逆反应活化能大100kJ·mol-1 |
已知4NH3 + 5O2 4NO + 6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是
4NO + 6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是
| A.4 v(NH3)=5v(O2) | B.6 v(O2)= 5v(H2O) |
| C.4v(NH3)="6" v(H2O) | D.v(O2)= 4v(NO) |
某反应的△H=+100k J·mol-1,下列有关该反应的叙述正确的是
J·mol-1,下列有关该反应的叙述正确的是
| A.正反应活化能小于100kJ·mol-1 | B.逆反应活化能一定小于100kJ·mol-1 |
| C.逆反应活化能不小于100kJ·mol-1 | D.正反应活化能比逆反应活化能大100kJ·mol-1 |
某密闭容器 中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g)
中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是
| A.30min时降低温度,40min时升高温度 |
| B.8min前A的平均反应速率为0.08mol/(L·s) |
| C.反应方程式中的x=1,正反应为吸热反应 |
| D.20min~40min间该反应的平衡常数均为4 |
对下列物质:①H2SO4、②CO2、③NaOH、④BaSO4、⑤NH3、⑥SO2、⑦NH3·H2O 、⑧C2H5OH、⑨Cu、⑩氯化钠溶液按要求分类不正确的是
| A.弱电解质:④、⑦ | B.电解质:①、 ③、④、⑦ ③、④、⑦ |
| C.非电解质:②、⑤、⑥、⑧ | D.强电解质:①、③、④ |
250℃和1.01×105Pa时,反应:2N2O5(g)=4NO2(g)+O2(g) △H=+56.76kJ/mol,自发进行的原因是
| A.是吸热反应 | B.是放热反应 |
| C.是熵减少的反应 | D.熵增大效应大于能量效应 |
将浓度为0.1mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是
| A.c(H+) | B. |
C.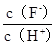 |
D.Ka(HF) |
下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B .CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol
.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
已知下列两个热化学方程式,实验测得氢气和丙烷的混合气体共5 mol,完全燃烧时放热3 847 kJ,则混合气体中氢气与丙烷的体积比是( )
2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol,
C3H8(g)+5O2(g)===4H2O(l)+3CO2(g) ΔH=-2 220.0 kJ/mol。
| A.3∶1 | B.1∶3 | C.1∶4 | D.1∶1 |
在298 K、100 kPa时,已知:
2H2O(g)===O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)="==2HCl(g) " ΔH2
2Cl2(g)+2H2O(g)===4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是( )
| A.ΔH3=ΔH1-2ΔH2 | B.ΔH3=ΔH1+ΔH2 |
| C.ΔH3=ΔH1+2ΔH2 | D.ΔH3=ΔH1-ΔH2 |
反应2A(g)  2B(g)+C(g) ⊿H> 0,达到平衡时,要使逆反应速率降低,A的浓
2B(g)+C(g) ⊿H> 0,达到平衡时,要使逆反应速率降低,A的浓 度增大,应采取的措施是
度增大,应采取的措施是
| A.减压 | B.加压 | C.降温 | D.增大B的浓度 |
低脱 硝技术可用于处理废气中的
硝技术可用于处理废气中的 氮氧化物,发生
氮氧化物,发生 的化学反应为:
的化学反应为:
2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g)
2N2(g)+3H2O(g)  H<0
H<0
在恒容的密闭容器中,下列有关说法正确的是
| A.单位时间内消耗NO和N2的物质的量比为1∶2时,反应达到平衡 |
| B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
某密闭容器中充入一定量A、B,发生反应2A(g)+B(g) 2C(g),测得C浓度与反应温度关系如图。下列说法正确的是
2C(g),测得C浓度与反应温度关系如图。下列说法正确的是
A.该反应ΔH>0  B.
B. A的转化率:a>b>c
A的转化率:a>b>c
C.平衡常数K:c>b>a D.化学反应速率:c>b>a
某温度下,在一容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
A.均减半 B.均增加1 mol C.均加倍 D.均减少1 mol
把煤作为燃料可以通过下列两种途径:
途径I:C(s)+O2(g) CO2(g) ΔH=E1 ①
CO2(g) ΔH=E1 ①
途径II:先制水煤气:C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②
再燃烧水煤气:H2(g)+1/2O2(g) H2O(g) ΔH=E3 ③
H2O(g) ΔH=E3 ③
CO(g)+1/2O2(g) CO2(g) ΔH=E4④ ,试回答下列问题:
CO2(g) ΔH=E4④ ,试回答下列问题:
(1)判断两种途径放热:途径I放出的热量 _____(填“大于”、“等于”、“小于”)途径II放出的热量。
_____(填“大于”、“等于”、“小于”)途径II放出的热量。
(2)E1、E2、E3、E4的数学关系式 是_____________________________________。
是_____________________________________。
(3)由于制取水煤气反应里,反应物所具有的总能量_______(填“大于”、“等于”、“小于”)生成物所具有的总能量,正反应又是熵增加的反应,为了让该反应自发进行,要使反应条件为_______。
25℃时,①醋酸②次氯酸③氢氟酸的电离常数分别是1.8×10-5、3.0×10-8、3.5×10-4。请推测:
(1)它们的酸性由强到弱的顺序为______________________(填序号,下同),
(2)相同浓度的溶液中,氢离子浓度最大的是___________;
(3)氢离子浓度相同的溶液中,酸的浓度最大的是 。
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH= kJ·mol-1。
SO3(g)+NO(g)的ΔH= kJ·mol-1。
(2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K= 。(保留2位小数)
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
CO在不同温度下的平衡转化率与压强的关系如图所示。
该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。

(1)已知某温度下,反应2SO2+O2 2SO3,的平衡常数K=19,在该温度下的体积
2SO3,的平衡常数K=19,在该温度下的体积 固定的密闭容器中充
固定的密闭容器中充 入C(SO2)=1mol·L-1,C(O2)="1" mol·L-1,当反应在该温度下SO2转化率
入C(SO2)=1mol·L-1,C(O2)="1" mol·L-1,当反应在该温度下SO2转化率 为80%时,该反应
为80%时,该反应
(填“是”或“否”)达到化学平衡状态,若未达到,向  (填“正反应”或“逆反应”) 方向进行。
(填“正反应”或“逆反应”) 方向进行。
(2)对于可逆反应:aA(g) +bB(g)  cC(g)+dD(g) △H = a kJ·mol
cC(g)+dD(g) △H = a kJ·mol -1;
-1;
若增大压强平衡向正反应方向移动,则a+b c+d(填“>”或“<”);若升高温度,平衡向正反应方向移动,则a_______0(填“>”或“<”)
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(图 中的ΔH表示生成1 mol产物的数据)。
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热 化学方程式是_________________________________;
化学方程式是_________________________________;
(2)PCl5分解成PCl3和Cl2的热化学方程式是_________________________________;
(3)上述分解反应是一个可逆反应。温度T1时,在密闭容器中加入0.80 mol PCl5,反应达平衡时PCl5[来还剩0.60 mol,其分解率α1等于________;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,
α2________α1(填“大于”、“小于”或“等于”)
已知分解100 g CaCO3需要177.7 kJ的热量,而12 g碳完全燃烧,则放出393 kJ的热。求:
(1)煅烧1 t石灰石需要多少热量?
(2)这些热量 全部由碳燃烧提供,问理论上要消耗多少克碳?
全部由碳燃烧提供,问理论上要消耗多少克碳?
 2NH3(g) △H<0,下列探究目的和示意图相符的是
2NH3(g) △H<0,下列探究目的和示意图相符的是

 91% ,求:
91% ,求: 粤公网安备 44130202000953号
粤公网安备 44130202000953号