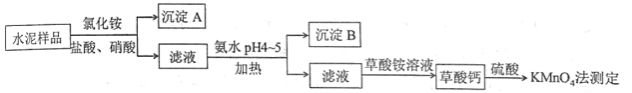
水泥是重要的建筑材料。水泥熟料的主要成分为 、 ,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是__________,还可使用___________代替硝酸。
(2)沉淀A的主要成分是_________________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为____________________________________。
(3)加氨水过程中加热的目的是___________。沉淀B的主要成分为_____________、____________(写化学式)。
(4)草酸钙沉淀经稀 处理后,用 标准溶液滴定,通过测定草酸的量可间接获知钙的含 量,滴定反应为: 。实验中称取 水泥样品,滴定时消耗了 的 溶液 ,则该水泥样品中钙的质量分数为______________。
由下列实验及现象不能推出相应结论的是( )
|
实验 |
现象 |
结论 |
|
|
A. |
向 的 溶液中加足量铁粉,振荡,加1滴KSCN溶液 |
黄色逐渐消失,加KSCN溶液颜色不变 |
还原性: |
|
B. |
将金属钠在燃烧匙中点燃,迅速伸入集满 的集气瓶 |
集气瓶中产生大量白烟,瓶内有黑色颗粒产生 |
具有氧化性 |
|
C. |
加热盛有少量 固体的试管,并在试管口放置湿润的红色石蕊试纸 |
石蕊试纸变蓝 |
显碱性 |
|
D. |
向2支盛有 相同浓度银氨溶液的试管中分别加入2滴相同浓度的 和 溶液 |
一只试管中产生黄色沉淀,另一支中无明显现象 |
|
重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为 ,还含有硅、铝等杂质。制备流程如图所示:

回答下列问题:
(1)步骤①的主要反应为:
上述反应配平后 与 的系数比为________。该步骤不能使用陶瓷容器,原因是________。
(2)滤渣1中含量最多的金属元素是________,滤渣2的主要成分是________及含硅杂质。
(3)步骤④调滤液2的 使之变________(填"大"或"小"),原因是________(用离子方程式表示)。
(4)有关物质的溶解度如图所示。向"滤液3"中加入适量 ,蒸发浓缩,冷却结晶,过滤得到 固体。冷却到________(填标号)得到的 固体产品最多。
a.
b.
c.
d.
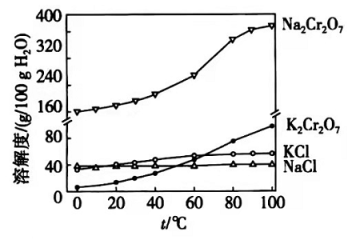
步骤⑤的反应类型是________。
(5)某工厂用 铬铁矿粉(含 40%)制备 ,最终得到产品 ,产率为________。
化学与生活密切相关。下列说法错误的是( )
| A. |
是指粒径不大于 的可吸入悬浮颗粒物 |
| B. |
绿色化学要求从源头上消除或减少生产活动对环境的污染 |
| C. |
燃煤中加入 可以减少酸雨的形成及温室气体的排放 |
| D. |
天然气和液化石油气是我国目前推广使用的清洁燃料 |
高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
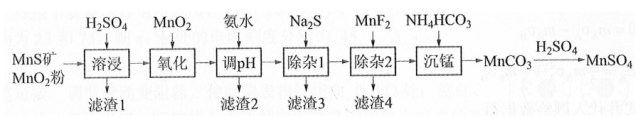
相关金属离子[ ]形成氢氧化物沉淀的pH范围如下:
|
金属离子 |
|
|
|
|
|
|
|
|
开始沉淀的pH |
8.1 |
6.3 |
1.5 |
3.4 |
8.9 |
6.2 |
6.9 |
|
沉淀完全的pH |
10.1 |
8.3 |
2.8 |
4.7 |
10.9 |
8.2 |
8.9 |
(1)"滤渣1"含有S和________;写出"溶浸"中二氧化锰与硫化锰反应的化学方程式________。
(2)"氧化"中添加适量的 的作用是将________。
(3)"调pH"除铁和铝,溶液的pH范围应调节为________~6之间。
(4)"除杂1"的目的是除去 和 , "滤渣3"的主要成分是________。
(5)"除杂2"的目的是生成 沉淀除去 。若溶液酸度过高, 沉淀不完全,原因是________。
(6)写出"沉锰"的离子方程式________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为 , 其中Ni、Co、Mn的化合价分别为+2、+3、+4。当 时, z=________。
下列实验不能达到目的的是( )
|
选项 |
目的 |
实验 |
|
A |
制取较高浓度的次氯酸溶液 |
将 通入碳酸钠溶液中 |
|
B |
加快氧气的生成速率 |
在过氧化氢溶液中加入少量 |
|
C |
除去乙酸乙酯中的少量乙酸 |
加入饱和碳酸钠溶液洗涤、分液 |
|
D |
制备少量二氧化硫气体 |
向饱和亚硫酸钠溶液中滴加浓硫酸 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
化学与生活密切相关。下列叙述错误的是( )
A. 高纯硅可用于制作光感电池 B. 铝合金大量用于高铁建设
C. 活性炭具有除异味和杀菌作用 D. 碘酒可用于皮肤外用消毒
下列化学方程式中,不能正确表达反应颜色变化的是( )
| A. |
向 溶液中加入足量Zn粉,溶液蓝色消失: |
| B. |
澄清的石灰水久置后出现白色固体: |
| C. |
在空气中放置后由淡黄色变为白色: |
| D. |
向 悬浊液中滴加足量 溶液出现红褐色沉淀: |
下列实验现象与实验操作不相匹配的是( )
|
实验操作 |
实验现象 |
|
|
A |
向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置 |
溶液的紫色逐渐褪去,静置后溶液分层 |
|
B |
将镁条点燃后迅速伸入集满 的集气瓶 |
集气瓶中产生浓烟并有黑色颗粒产生 |
|
C |
向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 |
有刺激性气味气体产生,溶液变浑浊 |
|
D |
向盛有 溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 |
黄色逐渐消失,加KSCN后溶液颜色不变 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1) 的化学名称是________。
(2)利用" 氧化法"制备 工艺流程如下图所示:

"酸化反应"所得产物有 、 和 。"逐 "采用的方法是________。"滤液"中的溶质主要是________。"调pH"中发生反应的化学方程式为________。
(3) 也可采用"电解法"制备,装置如图所示。
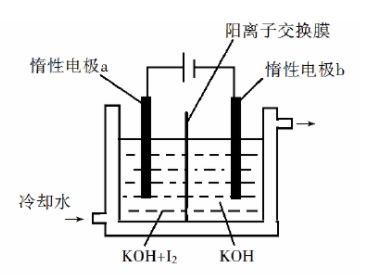
①写出电解时阴极的电极反应式________。
②电解过程中通过阳离子交换膜的离子主要为________,其迁移方向是________。
③与"电解法"相比," 氧化法"的主要不足之处有________(写出一点)。
硫代硫酸钠晶体(
)可用作定影剂、还原剂。回答下列问题:
(1)已知: , 。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
试剂:稀盐酸、稀 、 溶液、 溶液、 溶液
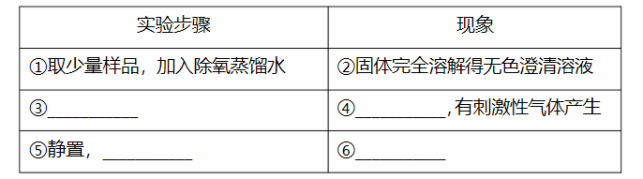
(2)利用 标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制:称取 某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在________中溶解,完全溶解后,全部转移至 的________中,加蒸馏水至________。
②滴定:取 的 标准溶液 ,硫酸酸化后加入过量KI,发生反应: 。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应: 。加入淀粉溶液作为指示剂,继续滴定,当溶液________,即为终点。平行滴定3次,样品溶液的平均用量为 ,则样品纯度为________%(保留1位小数)。
W、X、Y、Z均为短周期元素且原子序数依次增大,元素X和Z同族。盐YZW与浓盐酸反应,有黄绿色气体产生,此气体同冷烧碱溶液作用,可得到YZW的溶液。下列说法正确的是( )
| A. |
原子半径大小为W<X<Y<Z |
B. |
X的氢化物水溶液酸性强于Z的 |
| C. |
Y 2W 2与ZW 2均含有非极性共价键 |
D. |
标准状况下W的单质状态与X的相同 |
(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图,回答下列问题:
(1)晒制蓝图时,用 作感光剂,以 溶液为显色剂.其光解反应的化学方程式为 ,显色反应的化学方程式为________.
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下面所示装置进行实验。
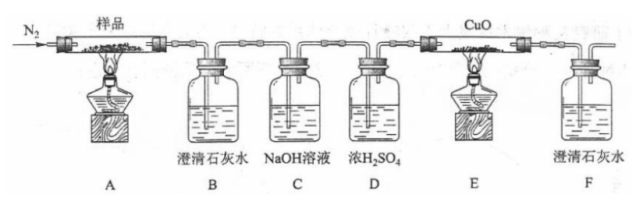
①通入氮气的目的是________。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有________、________。
③为防止倒吸,停止实验时应进行的操作是________。
④样品完全分解后,装置A中的残留物含有 和 ,检验 存在的方法是:________。
(3)测定三草酸合铁酸钾中铁的含量。
①称量 样品于锥形瓶中,溶解后加稀 酸化,用 溶液滴定至终点。滴定终点的现象是________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中,加稀 酸化,用 溶液滴定至终点,消耗 溶液 ,该晶体中铁的质量分数的表达式为________。
我国是世界上最早制得和使用金属锌的国家。一种以闪锌矿(ZnS,含有  和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:

相关金属离子  形成氢氧化物沉淀的pH范围如下:
形成氢氧化物沉淀的pH范围如下:

回答下列问题:
(1)焙烧过程中主要反应的化学方程式为________。
(2)滤渣1的主要成分出 外还有________;氧化除杂工序中ZnO的作用是________.若不通入氧气,其后果是________。
(3)溶液中的 可用锌粉除去,还原除杂工序中反应的离子方程式为________。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为________;沉积锌后的电解液可返回________工序继续使用。