环戊二烯(  )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
(1)已知: 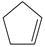 (g) =
(g) = 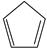 (g)+H 2(g) Δ H 1=100.3kJ·mol −1 ①
(g)+H 2(g) Δ H 1=100.3kJ·mol −1 ①
H 2(g)+ I 2(g) =2HI(g) Δ H 2=−11.0 kJ·mol −1 ②
对于反应:  (g)+ I 2(g) =
(g)+ I 2(g) = 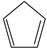 (g)+2HI(g) ③ Δ H 3=________kJ·mol −1。
(g)+2HI(g) ③ Δ H 3=________kJ·mol −1。
(2)某温度下,等物质的量的碘和环戊烯( 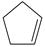 )在刚性容器内发生反应③,起始总压为10 5Pa,平衡时总压增加了20%,环戊烯的转化率为________,该反应的平衡常数 K p=________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有________(填标号)。
)在刚性容器内发生反应③,起始总压为10 5Pa,平衡时总压增加了20%,环戊烯的转化率为________,该反应的平衡常数 K p=________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有________(填标号)。
| A. |
通入惰性气体 |
B. |
提高温度 |
| C. |
增加环戊烯浓度 |
D. |
增加碘浓度 |
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是__________(填标号)。
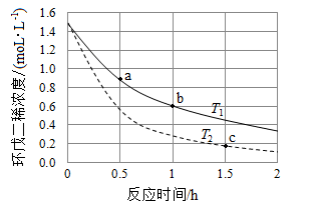
| A. |
T 1> T 2 |
| B. |
a点的反应速率小于c点的反应速率 |
| C. |
a点的正反应速率大于b点的逆反应速率 |
| D. |
b点时二聚体的浓度为0.45 mol·L −1 |
(4)环戊二烯可用于制备二茂铁(Fe(C 5H 5) 2结构简式为  ),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
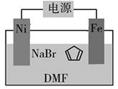

该电解池的阳极为________,总反应为________。电解制备需要在无水条件下进行,原因为________。
近期发现, 是继NO、CO之后第三个生命体系气体信号分子,它具有参与调解神经信号传递、舒张血管减轻高血压的功能.回答下列问题:
(1)下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是(填标号).
| A. |
氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以 |
| B. |
氢硫酸的导电能力低于相同浓度的亚硫酸 |
| C. |
的氢硫酸和亚硫酸的pH分别为4.5和2.1 |
| D. |
氢硫酸的还原性强于亚硫酸 |
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理.

通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为________、________,制得等量H 2所需能量较少的是________.
(3) 与 在高温下发反应:生 .在610k时,将 与 充入2.5L的空钢瓶中,反应平衡后水的物质的量分数为0.02.
① 的平衡转化率 =________%,反应平衡常数K=________.
②在620K重复试验,平衡后水的物质的量分数为0.03, 的转化率 ________ , 该反应的△H________0.(填">""<"或"=")
③向反应器中再分别充入下列气体,能使 转化率增大的是________(填标号)
| A. |
|
B. |
|
C. |
COS |
D. |
|
元素铬(Cr)在溶液中主要以 (蓝紫色)、 (绿色)、 (橙红色)、 (黄色)等形式存在, 为难溶于水的灰蓝色固体, 回答下列问题:
(1) 与 的化学性质相似,在 溶液中逐滴加入 溶液直至过量, 可观察到的现象是 。
(2) 和 在溶液中可相互转化。室温下,初始浓度为 的 溶液中 随 的变化如图所示。

①用离子方程式表示 溶液中的转化反应____________。
②由图可知,溶液酸性增大, 的平衡转化率__________(填"增大"减小"或"不变")。根据A点数据,计算出该转化反应的平衡常数为__________。
③升高温度,溶液中 的平衡转化率减小,则该反应的 _________(填"大于""小于"或"等于")。
(3)在化学分析中采用 为指示剂,以 标准溶液滴定溶液中的Cl −,利用Ag +与 生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好完全沉淀(浓度等于 )时,溶液中 为_______ ,此时溶液中 等于__________ 。(已知 、 的 分别为 和 )。
(4)+6价铬的化合物毒性较大,常用 将废液中的 还原成 ,反应的离子方程式为______________。
探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=﹣49.5 kJ•mol﹣1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g)△H2=﹣90.4 kJ•mol﹣1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g)△H3
回答下列问题:
(1)△H3= kJ•mol﹣1。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1mol CO2和3mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的浓度为 mol•L﹣1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为 。
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。
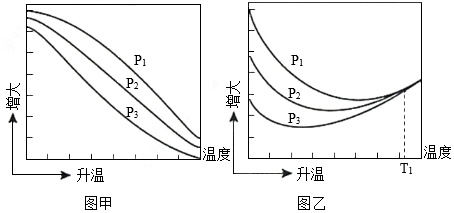
已知:CO2的平衡转化率 100%
CH3OH的平衡产率 100%
其中纵坐标表示CO2平衡转化率的是图 (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为 ;图乙中T1温度时,三条曲线几乎交于一点的原因是 。
(4 )为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为 (填标号)。
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
硫酸是一种重要的基本化工产品。接触法制硫酸生产中的关键工序是SO 2的催化氧化:SO 2(g) O 2(g) SO 3(g)△H=﹣98kJ•mol ﹣ 1.回答下列问题:
(1)钒催化剂参与反应的能量变化如图(a)所示,V 2O 5(s)与SO 2(g)反应生成VOSO 4(s)和V 2O 4(s)的热化学方程式为: 。
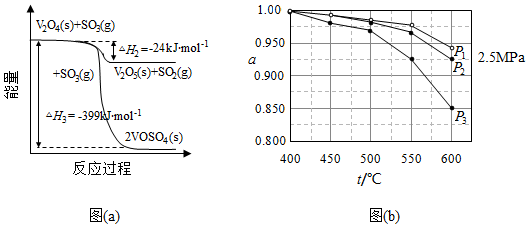
(2)当SO 2(g)、O 2(g)和N 2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO 2平衡转化率α随温度的变化如图(b)所示。反应在5.0MPa、550℃时的α= ,判断的依据是 。影响α的因素有 。
(3)将组成(物质的量分数)为2m% SO 2(g)、m% O 2(g)和q% N 2(g)的气体通入反应器,在温度t、压强p条件下进行反应。平衡时,若SO 2转化率为α,则SO 3压强为 ,平衡常数K p= (以分压表示,分压=总压×物质的量分数)。
(4)研究表明,SO 2催化氧化的反应速率方程为:v=k( 1) 0.8(1﹣nα′)式中:k为反应速率常数,随温度t升高而增大;α为SO 2平衡转化率,α′为某时刻SO 2转化率,n为常数。在α′=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图(c)所示。

曲线上v最大值所对应温度称为该α′下反应的最适宜温度t m.t<t m时,v逐渐提高;t>t m后,v逐渐下降。原因是 。