某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数,先将10g样品放入烧杯中,再把100g稀盐酸分5次加入该样品中(该实验条件下,杂质不与酸反应,也不溶解于水,忽略稀盐酸挥发),得实验数据如表格。
|
稀盐酸的质量 |
充分反应后剩固体的质量 |
|
第一次加入20g |
8g |
|
第二次加入20g |
6g |
|
第三次加入20g |
4g |
|
第四次加入20g |
2g |
|
第五次加入20g |
2g |
请计算;
(1)10g石灰石样品中碳酸钙的质量分数是 。
(2)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
(1)如图1为实验室制取并收集气体的装置图,请回答下列问题。
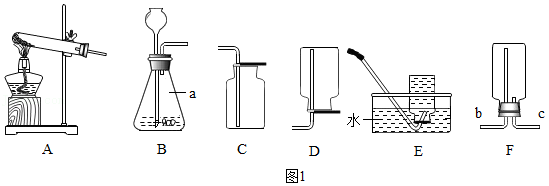
①仪器a的名称是 。
②若用A装置制取氧气,写出对应的化学方程式 。
③若需收集一瓶较纯净的氧气,应选用的装置是 (填装置序号)。
④若用C装置收集一瓶二氧化碳气体,其验满的方法是 。
⑤二氧化硫是一种有刺激性气味的有毒气体,比空气的密度大,易溶于水且与水反应。若用F装置收集二氧化硫气体,则气体应从 (填“b”或“c”)端导入。
(2)电解饱和食盐水可以制得氢氧化钠、氯气(Cl2)和氢气,并进而生产具有消毒、漂白作用的漂白液。
①粗盐中的难溶性杂质可通过溶解、 操作除去,以免破坏电解装置。
②写出电解饱和食盐水的化学方程式 。
③某同学想知道某一瓶放置一段时间的漂白液是否变质,设计了下列探究实验。
【查阅资料】
Ⅰ.制取漂白液(有效成分为NaClO)的原理:Cl2+2NaOH═NaCl+NaClO+H2O;
Ⅱ.在空气中NaClO易发生反应:2NaClO+H2O+CO2═Na2CO3+2HClO,HClO能使有色布条褪色,且HClO含量越高,漂白效果越好;HClO易分解,分解后丧失漂白作用;
Ⅲ.Ca(ClO)2易溶于水。
【提出问题】放置一段时间的漂白液是否变质?
【提出猜想】
猜想1:未变质,溶液中主要成分为NaCl、NaClO
猜想2:部分变质,溶液中主要成分为NaCl、NaClO、Na2CO3
猜想3:全部变质,溶液中主要成分为NaCl、Na2CO3
【实验探究】
|
实验操作 |
实验现象 |
实验结论 |
|
ⅰ取适量该溶液于烧杯中,放入有色布条 |
|
猜想3不成立 |
|
ⅱ另取适量该溶液于试管中,滴入适量氯化钙溶液 |
产生白色沉淀 |
猜想 成立 |
写出实验操作ii中产生白色沉淀的化学方程式 。
【拓展应用】由【查阅资料】和图2可知,需控制pH约为 时(填整数),漂白液具有最佳漂白能力。

阅读下面科普短文
2020年3月8日,面对口罩核心材料熔喷布的需求井喷,国务院国资委指导推动相关中央企业加快生产线建设,为新冠肺炎疫情防控提供保障。
熔喷布主要以聚丙烯[(C3H6)n]为原料,纤维直径可以达到1~5微米,具有独特的毛细结构超细纤维,从而使熔喷布具有很好的过滤性、屏蔽性、绝热性和吸油性,是良好的口罩材料。
聚丙烯是丙烯(C3H6)的聚合物。全球丙烯的工业化生产工艺主要有裂解法、催化裂化法(FCC),甲醇制烯烃(MTO/MTP)、丙烷脱氢(PDH)和烯烃歧化法等,我国和全球丙烯的工业化生产工艺方法及份额分别如图1、图2所示:

中国丙烯产能扩张速度稳定,未来产能增量以PDH为主,因PDH的主要成本来自于原料丙烷,丙烷价格越低廉,项目盈利越可观。因此丙烯作为化工领域中重要的基础原料产品,合理布局及发展烯烃产业结构尤为重要。
依据文章内容,回答下列问题:
(1)口罩的核心材料熔喷布主要以 为原料,它是有机合成材料,而日常生活中用得最多的有机合成材料是塑料、 、合成橡胶。
(2)熔喷布是良好的口罩材料,是因为它具有很好的 、 等优点(任写两点)。
(3)写出丙烯完全燃烧的化学方程式 。
(4)一定条件下,丙烷气体(C3H8)分解可以制得丙烯气体,写出该反应的化学方程式 。
(5)我国生产丙烯份额最多的方法是 ;由图2可知2015﹣2025年,全球各地区采用裂解和FCC生产丙烯份颜均有下降趋势,而 工艺法所产丙烯份额有逐步上升趋势。
金属材料与人类生活息息相关,请回答下列问题。
(1)钛元素在元素周期表中的信息如图所示,则钛的相对原子质量是 。
(2)家用台灯通常采用铜质插头,是利用金属铜的 性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是 。
(4)将一定质量的Zn片加入AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是 ;若滤液蓝色,则滤液中溶质一定有 。
化学就在我们身边,人类的衣、食、住、行都离不开化学。
(1)杂交水稻之父袁隆平说“人就像一粒种子,要做一粒好的种子”、水稻种子的主要成分为淀粉,淀粉属于 营养物质。
A.蛋白质
B.糖类
C.油脂
D.维生素
(2)碱性甲烷燃料电池具有低污染、高效率等特点,是一种很有前途的能源利用方式。
①电池总反应方程式为CH4+2O2+2KOH═K2CO3+3X,则X的化学式为 。
②K2CO3属于 类化合物(填物质类别),其中碳元素化合价为 。
(3)4500L氧气可加压装入容积为30L钢瓶中,其原因是 (从微观角度解)。
(4)在农业生产中,改良酸性土壤(硫酸型酸雨所致),通常加入 ,以中和其酸性,反应的化学方程式为 ,该反应属于 (填基本反应类型)。
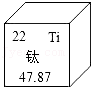
(1)如图1中A、B、C、D是四种粒子的结构示意图。
①C粒子的符号为 。
②图A、B、C、D共表示 种元素,由A、C两种元素组成的化合物的化学式为 。
③D中x= 。
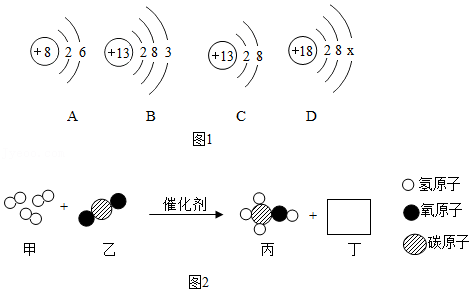
(2)二氧化碳会引起温室效应。某纳米纤维化剂可将二氧化碳转化为液体燃料甲醇(CH3OH),其微观示意图如图2(图中的微粒恰好完全反应)。
①该反应中涉及到的单质的化学式为 。
②写出该化学反应方程式: 。
下列图像能正确反应其对应关系的是( )
A.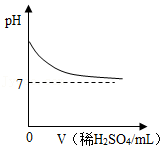 表示向一定质量的Ba(OH)2溶液中逐滴加入稀H2SO4至过量
表示向一定质量的Ba(OH)2溶液中逐滴加入稀H2SO4至过量
B.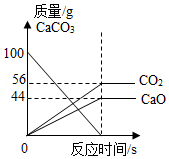 表示发生的反应为:CaCO3
表示发生的反应为:CaCO3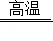 CaO+CO2↑
CaO+CO2↑
C. 表示等质量且过量的锌粉和铁粉,分别与质量和质量分数都相同的稀硫酸反应
表示等质量且过量的锌粉和铁粉,分别与质量和质量分数都相同的稀硫酸反应
D. 表示向盛有MnO2的烧杯中加入H2O2溶液
表示向盛有MnO2的烧杯中加入H2O2溶液
《中国诗词大会》弘扬了中国传统文化,下列诗句反映的物质变化主要为化学变化的是( )
| A. |
千淘万漉虽辛苦,吹尽狂沙始到金 |
| B. |
千锤万凿出深山,烈火焚烧若等闲 |
| C. |
花气袭人知骤暖,鹊声穿树喜新晴 |
| D. |
无边落木萧萧下,不尽长江滚滚来 |
常温下,一锥形瓶中盛有10g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,再逐滴滴加一定溶质质量分数的稀盐酸,用pH传感器测得溶液pH与加入稀盐酸的关系曲线如图所示,请回答下列问题:
(1)图中B点溶液呈 色。
(2)计算稀盐酸中溶质质量分数。(写出计算过程)
2009年,我国华为公司推出了5G商用芯片,制造芯片要用到高纯硅,如图为制备高纯硅和二氧化硅的主要工艺流程。

(1)反应①从基本反应类型角度分析,该反应属于 反应。
(2)反应②的化学方程式为 ,该工艺流程中可以循环利用的物质是 。
“珍爱生命,远离毒品”,冰毒是一种危害性很大的毒品,其主要成分是甲基苯丙胺(化学式为C10H15N)。某化学学习小组模拟对毒品的销毁,利用所制得的氧气燃烧冰毒,并检验所生成的二氧化碳气体,设计了如图实验。

本次实验只提供了如下化学试剂:5%的过氧化氢溶液,二氧化锰固体,浓硫酸,NaOH溶液,Ca(OH)2溶液,冰毒。请回答下列问题:
(1)仪器a的名称是 。
(2)为了完成此实验,除了选择装置B以外,还应选择的装置组合是 (填装置序号字母)。
(3)连接好装置,在加入药品前还必须进行的操作是 。
(4)检验二氧化碳时所发生反应的化学方程式为 。
酸、碱、盐在生产生活中具有广泛的用途。
(1)化学实验室有失去标签的硝酸钡、碳酸钠、氢氧化钾、稀硫酸、氢氧化钙五瓶无色溶液,现将其任意编号A、B、C、D、E,然后两两混合进行实验,其部分现象如下表(微溶物视为可溶物)。
|
实验 |
A+E |
A+B |
B+C |
B+E |
|
现象 |
产生沉淀 |
产生沉淀 |
产生沉淀 |
产生气体 |
①碳酸钠俗称纯碱,属于 类(填字母序号)。
A.酸
B.碱
C.盐
②写出溶液B中溶质的化学式 。
③写出溶液A与E反应的化学方程式 。
(2)我国制碱工业先驱侯德榜发明了“侯氏制碱法”,其主要化学原理:NaCl+H2O+NH3+CO2═NaHCO3↓+X;2NaHCO3 Na2CO3+H2O+CO2↑等。则X的化学式为 。
Na2CO3+H2O+CO2↑等。则X的化学式为 。
如图所示的四个图像表示的变化趋势,分别对应四种操作过程,其中正确的是( )
A. 氢氧化钠溶液中加入足量的水稀释
氢氧化钠溶液中加入足量的水稀释
B. 加热一定量氯酸钾和二氧化锰的混合物
加热一定量氯酸钾和二氧化锰的混合物
C.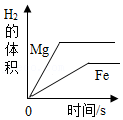 等质量的镁和铁与足量的稀硫酸反应
等质量的镁和铁与足量的稀硫酸反应
D.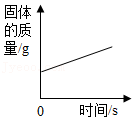 将一定质量的硫酸铜溶液倒入盛有铁钉的烧杯中
将一定质量的硫酸铜溶液倒入盛有铁钉的烧杯中
下列选项中关于性质或变化的说法正确的是( )
|
A. |
铁在潮湿环境中易生锈 |
化学性质 |
|
B. |
酒精挥发 |
化学变化 |
|
C. |
氧气用于急救病人 |
物理性质 |
|
D. |
木材燃烧 |
物理变化 |
A.AB.BC.CD.D
孔雀石的主要成分是Cu2(OH)2CO3,还含有Fe2O3、Al2O3、SiO2杂质,用该矿石制备Cu的流程如图所示(部分产物略去):
 (1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(2)过程①中硫酸略过量,则过程②调pH除杂的最佳试剂是 (选填“CuO”或“Na2CO3”)。
(3)下列关于制取铜的两种方案的说法,正确的是 。
A.“方案一”得到的铜产品更纯
B.“方案一”不存在消耗能量的问题
C.“方案二”需考虑废气污染的问题
D.“方案二”得到纯铜的产率更高
(4)过程③发生的反应:2CuSO4+2H2O 2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)