小明同学欲测定某纯碱样品(含少量氯化钠)中碳酸钠的质量分数,取26.5g该纯碱样品加入到100g水中,使其完全溶解,再加入169.3g稀盐酸,恰好完全反应,得到287g不饱和溶液。请计算:
(1)纯碱样品中碳酸钠的质量分数
(2)反应后得到的不饱和溶液中溶质的质量分数。
学习化学开启了我们认识物质之旅。某实验小组的同学对氢氧化钠的性质及应用进行了如下的探究。
[探究一]溶解过程中的能量变化
如图所示,同学们设计了不同的实验方案进行探究:

(1)实验一中的硝酸铵溶解后,溶液温度 (填"升高"、"降低"或"不变")。
(2)实验二所加试剂及用量如图,将分液漏斗中的水全部加入试管后,立即关闭分液漏斗的活塞,此时观察到U形管的液面左低右高,由此小明得出"氢氧化钠溶于水时放出热量"的结论,你是否同意小明的结论并写出你的理由 。
[探究二]氢氧化钠的化学性质
如图所示,同学们用氢氧化钠溶液进行了下列实验,请分析并回答下列问题:

(1)A试管中观察到的现象是 。
(2)B试管中发生反应的化学方程式: 。
(3)C、D试管中均无明显现象。
①为了证明D中已发生化学反应,向该试管中再加入足量的 ,观察到有气泡产生。
②为了证明氢氧化钠溶液和稀盐酸能发生化学反应,同学们设计并进行了如下实验:(所用稀盐酸经估算确保过量)

整个实验过程中无明显现象,证明氢氧化钠溶液和稀盐酸能发生化学反应。请写出步骤Ⅱ中所加试剂 。
[探究三]氢氧化钠的应用
(1)实验室中的应用
实验室中能用氢氧化钠溶液吸收的气体是 (填字母)。
a.二氧化碳
b.水蒸气
c.氯化氢
d.氧气
吸收上述所选气体,一般不用氢氧化钙溶液,主要是因为氢氧化钠和氢氧化钙的 不同。
(2)工业中的应用
氢氧化钠常用于制造人造丝、造纸、炼油、纺织、印染与橡胶工业。某造纸厂废水中NaOH的质量分数为1.6%,现有废硫酸4.9t(H 2SO 4的质量分数为20%),可以处理的废水质量是 t。
结合化学方程式中的数据分析:若将等质量、等溶质质量分数的稀硫酸和氢氧化钠溶液混合,充分反应后,请判断溶液中一定含有的溶质,并简述你的判断理由: 。
南通滨临长江,将长江水净化处理可成为居民生活用水。
(1)水净化时先加入絮凝剂,沉降过滤后,通过活性炭。活性炭的作用是 。
(2)将硬水通过如图所示的阳离子交换柱后可变成软水(图中阴离子未画出),交换后的水仍然呈电中性。
①一个Ca2+可以交换出 个Na+。
②阳离子交换柱长时间使用后,Na+变少,失去硬水软化功能而失效。利用生活中常见物质检验阳离子交换柱已失效的方法是 。
(3)二氧化氯(ClO2)可用于饮用水的杀菌消毒。取100mL经ClO2消毒后的饮用水于锥形瓶中,调节溶液至弱碱性,加入足量KI充分反应,测得生成I2的质量为0.0254mg。上述过程中发生的反应为2ClO2+2KI═2KClO2+I2,其他物质不参与反应。计算该饮用水中ClO2的残留量(以mg/L计),在答题卡上写出计算过程。

实验室里有一瓶氢氧化钙粉末由于较长时间敞口放置,已部分变质为碳酸钙。某课外兴趣小组为测定该瓶粉末中碳酸钙的质量分数,进行实验操作、数据收集和计算。
(1)配制稀盐酸:配制500克7.3%的稀盐酸,需要36.5%的浓盐酸 克。
(2)抽样测定:将瓶中粉末搅拌均匀后称取20克样品放入烧杯并置于电子秤上,再加入足量稀盐酸充分反应,总质量与反应时间的关系如下表所示:
| 反应时间/秒 |
0 |
10 |
20 |
30 |
40 |
| 总质量/克 |
310.0 |
309.6 |
308.6 |
307.8 |
307.8 |
完全反应后,生成的CO 2气体的质量为 克
(3)计算出该样品中CaCO 3的质量分数(要有计算过程)。
(4)经过分析讨论,同学们觉得这样测得的结果有可能偏大,原因是 (指出一点即可)
往100g硫酸和硫酸铜的混合液中,逐滴加入8%的氢氧化钠溶液直至过量,根据实验事实绘制了如图所示曲线,分析并计算:
(1)a→b段表示氢氧化钠与混合物中的 发生反应。
(2)求反应前混合液中硫酸铜的质量分数。(写出计算过程)

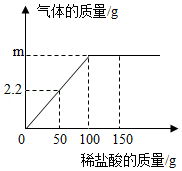
小苏打是发酵粉的主要成分之一,可用于制作发面食品。一化学兴趣小组对某小苏打样品中各成分的含量做了如下测定:将一定质量的该样品(已知杂质只含NaCl)加水全部溶解后,得到104.4g溶液,向该溶液中逐渐加入稀盐酸,产生的气体与加入稀盐酸的质量关系如图所示。试计算:
(1)m的值为 。
3与NaCl的质量比 。
黄铜是铜和锌的合金。某化学兴趣小组的同学欲测定实验室中某黄铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。称量10g粉末状黄铜样品放入烧杯中,量取45mL稀硫酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
| |
第一次 |
第二次 |
第三次 |
| 加入稀硫酸的体积(mL) |
15 |
15 |
15 |
| 生成氢气的质量(g) |
m |
0.04 |
0.02 |
试求:
(1)m的数值 。
(2)此黄铜样品中铜的质量分数是少?(写出计算过程)
欲测定盐酸与氯化钙的混合溶液中氯化钙的质量分数,进行了如下实验:取混合溶液100g于锥形瓶中,向其中逐渐加入一定溶质质量分数的碳酸钠溶液(如图一),并不断测定锥形瓶中溶液的pH.反应过程中所得溶液的pH与锥形瓶中物质的总质量的关系如图二所示。其中,当锥形瓶中溶液的质量增加至147.8g时,共消耗碳酸钠溶液的质量为50g。(忽略二氧化碳在水中溶解的量;氯化钙溶液显中性。)
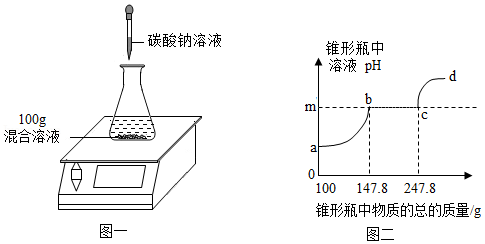
(1)m点的数值是 。
(2)a→b段表示碳酸钠与混合溶液中的 反应。
(3)参加反应的碳酸钠溶液的溶质的质量分数是 。
(4)请计算原混合溶液中CaCl 2的质量分数(写计算过程)。
工业合成氨的相关反应式为:N2+3H2 2NH3
(1)合成氨的原料气中可以通过分离空气直接得到的是 。
(2)当前,原料气H2可用天然气来制取,理论上每生产1吨H2会同时产生5.5吨CO2,有科学家正在研究一种不生成CO2的新方法来制取原料气H2.若需要合成8.5万吨氨,改用新方法制取原料气H2可以减少排放多少万吨CO2?
工业纯碱中常含有少量的氯化钠。某学习小组对其组成展开探究。现取24g纯碱样品,加入100g水使其完全溶解,再加入96g过量的氯化钙溶液,完全反应后,过滤、洗涤、干燥得沉淀20g。完成下列问题:
(1)反应后溶液中含有的溶质是 。(写化学式)。
(2)通过已知数据,能求出的量有 (写字母序号)。
A.反应后溶液的总质量
B.参加反应的氯化钙的质量
C.样品中碳酸钠的质量分数
D.氯化钙溶液中溶质的质量分数
(3)计算反应后溶液中氯化钠的质量分数。(写出计算过程,结果保留到0.1%)
某科学兴趣小组同学取8.5g铁,放到含少量硫酸的硫酸铜溶液中,完全反应后,最终得到9.2g固体。为测定所得固体中各成分的含量,同学们将62.5g稀盐酸分五次加入到该固体中,得到数据如表:
次数 |
1 |
2 |
3 |
4 |
5 |
加入盐酸溶液质量/g |
12.5 |
12.5 |
12.5 |
12.5 |
12.5 |
剩余固体质量/g |
8.5 |
7.8 |
a |
6.4 |
6.4 |
请分析计算:
(1)表中a的值是 。
(2)9.2g固体中铁的质量是 。
(3)稀盐酸的溶质质量分数是多少?
(4)与硫酸铜反应的铁的质量是多少?
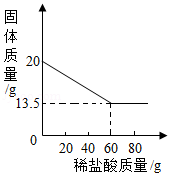
向20g铜锌合金中不断加入一定溶质质量分数的稀盐酸,加入稀盐酸的质量与固体质量的关系如图所示。请计算:
(l)合金中锌的质量分数为 。
(2)所用稀盐酸的溶质质量分数。(计算结果保留一位小数)
实验室用34克过氧化氢溶液和1克二氧化锰制取氧气,实验的相关数据如图。请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的 都没有发生变化。
(2)反应生成氧气的质量为 g。
(3)计算过氧化氢溶液中溶质的质量分数。(此问必须要有计算过程)
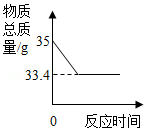
厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如图所示。
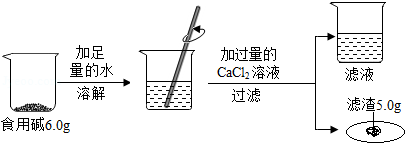
计算:该食用碱中碳酸钠的质量分数是多少?(计算结果精确至0.1%)