如图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器,欲利用其进行下列化学实验。

(1)用单质锌和稀硫酸反应,制取氢气并进行氢气可燃性实验。在点燃氢气前,一定要注意检验 。
(2)以石灰石和稀盐酸为原料制取二氧化碳的化学方程式为 。制取、收集干燥的二氧化碳气体,并去除混有的少量HCl气体,所选仪器的连接顺序为 (从左至右填写仪器序号字母)(提示:挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)。
(3)在实验室中以过氧化氢溶液为原料(二氧化锰作催化剂)制取氧气,并对某种塑料袋试样的组成元素进行分析探究(查阅资料知该塑料只含C、H两种元素),所选仪器按“A→E1→D→E2→B→碱石灰干燥管”的顺序连接(E1、E2为浓硫酸洗气瓶),实验前检验装置气密性。使一定质量的该塑料袋碎屑在氧气中充分燃烧,观察现象,收集有关实验数据(假设发生的化学反应都充分反应)。
①在该装置中,洗气瓶E1、E2的作用是 。
②仪器D的大玻璃管中放入的塑料袋碎屑质量为5.6g,加入的塑料袋碎屑充分燃烧后,测得仪器E2的质量增加7.2g,仪器B的质量增加17.6g,则在该塑料袋试样中,氢、碳两元素的质量之比为氢元素的质量:碳元素的质量= (填写最简整数比)。
2017年12月18日,南通地铁正式开建,标志着南通进入“地铁时代”。

(1)地铁列车车体大量使用的镁铝合金属于 (填“金属材料”或“合成材料”),镁铝合金的优点是 。
(2)地铁建造过程中需要使用大量的钢铁。工业炼铁可利用一氧化碳与氧化铁反应,写出该反应的化学方程式: 。
2)和晶体硅(Si)。将二氧化硅转化为硅的过程属于 (填“物理变化”或“化学变化”)。
(4)地铁施工过程中产生的废水、废浆以及机械漏油等,都会对水体产生污染。使用活性炭可对污水进行处理,这是利用了活性炭的 性。
(5)为确保消防安全,地铁隧道中须安装自动喷淋系统。喷出的水能灭火的原因是 。
(6)地铁施工工程车的尾气中含NO、CO.尾气经过如图2所示催化转化后,可实现达标排放。写出单质X的化学式: 。
自来水厂净化河水的主要步骤如图所示,请回答下列问题:

(1)下列物质属于纯净物的是 。
A、河水 B、蒸馏水 C、生理盐水 D、自来水
(2)通过图中Ⅰ可以除去河水中的 。
(3)图中Ⅱ加入的物质X是 (填名称)。
(4)图中Ⅲ加入的漂白粉可杀菌、消毒、工业上制取漂白粉的反应原理:2Ca(OH)2+2Cl2═Ca(ClO)2+M+2H2O,则M的化学式是 。
孔雀石的主要成分为Cu2(OH)2CO3,在加热条件下发生如下反应:Cu2(OH)2CO3 2R+CO2↑+H2O,请回答问题:
(1)R的化学式为 ;
(2)该反应属于 (填基本反应类型).
能源利用和环境保护是人类共同关注的问题。
(l)下列说法中正确的是 (填字母)。
A.煤、石油和天然气都属于可再生能源
B.从环境保护角度考虑,最理想的燃料是汽油
C.可燃冰将成为未来新能源,其中主要含有甲烷水合物
(2) 煤燃烧时排放出的二氧化硫等污染物, 有可能会导致降雨的酸性增强。 我们把pH 5.6(填“>”“=”或“<”)的降雨称为酸雨。某电厂为防止环境污染,用石灰石浆来吸收二氧化硫,其反应的化学方程式为:2CaCO3+2SO2+O2=2CaSO4+2x,则x的化学式为 。
(3)研究发现,二氧化碳和氢气在催化剂作用下转化为甲醇(CH3OH)和水。该反应的化学方程式为 。
(4)将一定质量的甲醇与4.4g氧气混合于密闭容器内,在一定条件下,发生如下反应:
8CH3OH+xO2 mCO2+nCO+16H2O.当反应物完全耗尽且全部转化为生成物时,有3.6g水生成,同时生成二氧化碳的质量为 g。
mCO2+nCO+16H2O.当反应物完全耗尽且全部转化为生成物时,有3.6g水生成,同时生成二氧化碳的质量为 g。
石灰石和铁的化合物在生产、生活中有着广泛的应用.
(1)炼铁的原理是一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,写出该反应的化学反应方程式 .
(2)牙膏中常用轻质碳酸钙粉末做摩擦剂.生产轻质碳酸钙的主要过程:①煅烧石灰石制得氧化钙; ②氧化钙加水制成石灰乳[主要成分是Ca(OH) 2]; ③石灰乳与二氧化碳反应得到碳酸钙.写出③的化学方程式 .
(3) 取62.5g含碳酸钙80%的石灰石(杂质不含钙元素且不参加反应)高温煅烧,一段时间后停止加热,测得剩余固体中钙元素的质量分数为40%,则生成的二氧化碳质量为 g.
(4)合成氨工业生产中所用到的催化剂是铁触媒,其主要的成分是FeO和Fe 2O 3,当FeO和Fe 2O 3中铁元素的质量比为1:2时,该催化剂的催化作用效果最好,此时FeO和Fe 2O 3的质量比为 (写最简比).
我国自主研制的首颗"碳卫星"将于2016年8月发射,主要任务是监测各地区二氧化碳的排放,为节能减排等宏观决策提供依据,请回答下列问题:
(1)大气中二氧化碳含量升高的一个主要原因是 燃料的大规模开发使用.
(2)固定和利用二氧化碳能有效减少空气中的温室气体.例如工业上利用CO 2和NH 3生产尿素的反应:CO 2+2NH 3  CO(NH 2) 2+X,则X的化学式为 .
CO(NH 2) 2+X,则X的化学式为 .
(3)下列行为符合"低碳生活,保护环境"这一理念的是 (填序号)
①焚烧纸质垃圾 ②步行上学 ③用电动牙刷刷牙.
阅读下列科普短文.
根据短文回答以下问题:
提到炸药,同学们可能会想到战争和暴力,但炸药的发明却促进了工业和经济的进步.我国是最早发明火药的国家,黑火药是我国古代的四大发明之一,主要分为硝酸钾、硫、木炭等.黑火药经点燃,发生剧烈燃烧,反应原理为:2KNO 3+S+3C K 2S+N 2↑+3CO 2↑
黑火药经阿拉伯传到欧洲,随后各国化学家陆续研制出各种炸药,如意大利化学家索布雷罗发明的硝化甘油,爆炸时威力很大,但安全性很低.瑞典化学家诺贝尔在前人研究的基础上,经过反复实验,研制出安全性很高的硝化甘油炸药,提高了它的利用价值.炸药的研发还在继续,安全烈性炸药不断问世,如TNT、黑索金等.
黑火药推动了炸药的快速发展,它虽然已退出军事领域,但依然发挥着重要的民用价值,如制造焰火、定向爆破等.我国近年来研制的纳米级黑索金,在理论和实验制备等方面获得了突破,将会继续在工业和军事领域做出贡献.
(1)黑火药不需外界提供氧气也可以发生爆炸,这是因为其成分中的 生成氧气的结果.
(2)通过阅读,下列说法正确的是 (填字母,符合题意的选项都选).
a.黑火药作为一种古老的炸药,现在已停止使用
b.黑火药能发生爆炸与它燃烧后生成气体并放出热量有关
c.使用危险物质时,我们应采取一些措施提高其安全性,更好地发挥其作用
(3)炸药属于易爆物,生活中我们有时会接触一些易爆物,下列建议正确的是 .
a.在加油加气站禁止打电话 b.夜晚发现家中燃气泄漏需要开灯检查.
化学就在我们身边,化学与生活息息相关.
(1)如表为某食品包装袋的部分说明:
商品名称 |
××饼干 |
配料 |
小麦粉、白砂糖、精炼植物油、鸡蛋、食盐、食品添加剂(碳酸氢铵、碳酸氢钠、柠檬酸等) |
规格 |
180g |
保持期 |
10个月 |
请回答下列问题:
①在饼干的配料中,富含蛋白质的是
②碳酸氢钠的俗称 ;在医疗上,它是治疗 症的一种药剂.
③考虑到营养均衡,把榨好的蔬菜汁放在面粉中和面,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的主要营养素是糖类和 .
(2)饮用硬度过大的水不利于人体健康,日常生活中常用 来区分硬水和软水,可用 的方法降低水的硬度.
325242433CHO+6X,X的化学式为 .
应用所学知识,分析有关信息,回答下列问题:

(1)最近我市完成了92号和95号汽油的推广使用,降低了汽车尾气中的硫氧化物,为进一步减少污染,通常在汽车的排气管上装一个"催化转换器".装置中发生反应的微观示意图如图所示:
请写出反应的化学方程式 ;
在反应前后化合价没有发生变化的元素是 .
(2)已知金属镁可以在某种气体中燃烧,用化学方程式表示为:2Mg+X  2MgO+C,则X的化学式为 ;若金属镁的质量为m 1,完全反应后生成碳的质量为m 2,则m 1 m 2(填>、=、<).
2MgO+C,则X的化学式为 ;若金属镁的质量为m 1,完全反应后生成碳的质量为m 2,则m 1 m 2(填>、=、<).
汽车尾气催化转化器的投入使用,可缓解大气污染。下图为其中某种转化的微观示意图。

(1)图中表示单质微粒的化学式 ;
(2)对此转化过程的认识,不正确的是 ;
A.催化剂是实现转化的条件 B.能减少碳元素排放量
C.催化剂能增加生成气体的产量 D.氮元素的化合价降低
(3)若某车辆汽车经燃烧产生如图I中气体的质量各为12g,实测相同时间经转化排放出的图Ⅱ中气体总质量为20.4g。某同学认为污染物没有完全转化,他的依据是 ,计算图I中某一种气体实际转化的质量是 g。
(1)通过初中阶段的学习,知道实验室中有多种途径可以制取氧气,如:①加热高锰酸钾②加热氯酸钾和二氧化锰的混合物 ③ .
(2)用如图所示实验装置加热高锰酸钾制氧气,下列实验步骤已按顺序排列,请你在⑦处补全还缺少的一个实验步骤.
①组装仪器 ②检查装置的气密性
③将药品装入试管 ④将试管固定在铁架台上
⑤点燃酒精灯给药品加热 ⑥收集气体
⑦ ⑧熄灭酒精灯
(3)加热高锰酸钾制氧气的装置中试管口要略向下倾斜的原因是 .
(4)用2N g的高锰酸钾加热,完全反应可制得氧气a g;如改用加热N g高锰酸钾和N g氯酸钾的混合物,完全反应可制得氧气b g;则a b(填“>、﹦或<”).
氧是地壳中含量最多的元素,氧及其化合物是化学学习和研究的重要内容。
(1)如图氧原子结构示意图获得的信息,正确的是 (填标号)。
a. 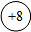 表示原子核,带8个单位正电荷
表示原子核,带8个单位正电荷
b.氧原子核外有2个电子层,有8个电子在核外作高速运动
c.氧原子在化学反应中易失去电子形成离子(O 2 ﹣)
(2)构成氧气的微粒是 ,氧气经降温和加压变为液态氧后体积变小,用微粒的观点解释: 。
(3)水是重要的氧化物,电解水实验说明水是由 组成的。登山和潜水供氧装置中,过氧化钠(Na 2O 2)与水反应,生成氢氧化钠(NaOH)和氧气,有关反应的化学方程式为 。
(4)自然界中氧循环的环节之一:绿色植物的光合作用,有关的化学方程式为6CO 2+6H 2O C 6H 12O 6+XO 2,则X= ,绿色植物通过光合作用将太阳能转化为 能。
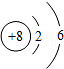
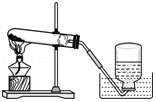
浓硫酸具有脱水性,能把小木棍、蔗糖等中的氢元素和氧元素“脱出”结合生成水。
(1)用小木棍蘸取浓硫酸少许,一段时间后,小木棍上出现的实验现象是 。
(2)在蔗糖(C12H22O11)分子中,氢、氧原子个数比是 ,如果蔗糖完全脱水,则生成C和H2O的质量比是 。
为了测定一瓶未密封保存的NaOH固体中NaOH的质量分数,小科采用沉淀法进行如下操作:①取15克样品于烧杯中,加足量水配成溶液;②在样品溶液中加入足量的BaCl2溶液;③待反应完全后,过滤。有关数据记录如表:
反应前 |
反应后 |
|
烧杯和样品溶液总质量/g |
加入的氯化钡溶液质量/g |
过滤后烧杯和溶液总质量/g(滤液的损失忽略不计) |
95 |
65 |
140.3 |
请回答下列问题:
(1)在反应前后的溶液中,下列元素质量保持不变的是
A.钠元素
B.碳元素
C.钡元素
D.氧元素
(2)反应共生成沉淀 克
(3)原样品中NaOH的质量分数是多少?