小英同学用某铁合金样品做了如下实验:称量11.4g样品,放入质量为40g的烧杯中,再往烧杯中加入200g稀硫酸,恰好完全反应(杂质不与酸反应,也不溶于水)。反应完毕后称量,烧杯及烧杯内物质总质量为251g。求:
(1)反应产生的氢气质量为 g;
(2)所用稀硫酸的溶质质量分数(写出计算过程)。
小苏打(NaHCO 3)是发酵粉的主要成分,可用于制作发面食品。化学兴趣小组为测定某品牌小苏打样品(含NaCl杂质)中碳酸氢钠的含量做了如下实验:将该样品17.1g放入锥形瓶中,加水全部溶解后,得到208.8g样品溶液,向该样品溶液中不断加入稀盐酸(如图),反应过程中锥形瓶中溶液质量的变化如下表所示。(忽略CO 2在水中的溶解)
| 加入稀盐酸的总质量/g |
25 |
50 |
75 |
| 锥形瓶中溶液的质量/g |
229.4 |
250 |
275 |
试计算:
(1)当加入25g稀盐酸时,产生二氧化碳的质量是 g。
(2)17.1g小苏打样品中NaHCO 3的质量(写出计算过程,下同)。
(3)当锥形瓶内样品溶液中的碳酸氢钠与加入的稀盐酸恰好完全反应时,锥形瓶中溶液的溶质质量分数。(计算结果精确至0.1%)

为了测定石灰石中碳酸钙的质量分数,现取12.5g石灰石(杂质不反应也不溶解)加入盛有105.4g稀盐酸的烧杯中,反应中烧杯内物质的质量与反应时间的关系如图所示,请计算:
(1)完全反应时生成二氧化碳多少克?
(2)石灰石中碳酸钙的质量分数是多少?
(3)完全反应时,所得溶液中溶质的质量分数是多少?

小嘉发现:向碳酸钠溶液中倾倒稀盐酸,很快就产生了气泡:向碳酸钠溶液中逐滴加入稀盐酸,滴加一定量后才有气泡产生。查阅资料:向碳酸钠溶液中逐滴加入稀盐酸,先发生的反应是Na2CO3+HCl═NaCl+NaHCO3;当Na2CO3全部转化成NaHCO3后,再发生反应NaHCO3+HCl═NaCl+H2O+CO2↑。为此他用如图所示装置进行了如下实验:
步骤一:在广口瓶中加入10克溶质质量分数为10.6%的碳酸钠溶液,用注射器向瓶中缓慢注入一定量的溶质质量分数为7.3%的稀盐酸,观察到瓶内无明显现象; 步骤二:继续用注射器向瓶中注入稀盐酸,一段时间后观察到瓶内连续产生气泡,烧杯中澄清石灰水?。 |
(1)步骤二中,观察到烧杯中澄清石灰水 。
(2)上述实验中,加入稀盐酸多少克后,才开始产生二氧化碳? 。
(3)向一定量碳酸钠溶液中无论是倾倒还是逐滴加入足量的稀盐酸,完全反应后产生二氧化碳质量是相同的,其本质原因是什么? 。

今天是某校实验室开放日,晓明同学用锌和稀硫酸反应制取氢气.先向气体发生装置中加入一定量的锌粒,然后将60克稀硫酸分三次加入,每次生成气体的质量如下表:
次数 |
第一次 |
第二次 |
第三次 |
加入稀硫酸质量/g |
20 |
20 |
20 |
生成氢气的质量/g |
0.08 |
0.08 |
0.04 |
试计算:
(1)共制得氢气 g.
(2)实验所用稀硫酸中溶质的质量分数.(写出计算过程)
菱镁矿中主要含MgCO3、FeCO3和SiO2.以菱镁矿为原料制取镁的工艺流程如图。
回答下列问题:
(1)菱镁矿属于 (选填“纯净物”或“混合物”)。
(2)流程中滤渣a主要成分是 。
(3)写出菱镁矿中MgCO3与稀HCl反应的化学方程式 。
(4)溶液b→溶液c反应的化学方程式为:4FeCl2+ +4HCl=4FeCl3+2H2O(补充完方程式)
(5)溶液c调pH使Fe3+完全沉淀为Fe(OH)3从而与Mg2+分离,则调pH的范围应为2.8﹣ 。
已知:物质沉淀的pH见下表:
物质 |
Mg(OH)2 |
Fe(OH)3 |
开始沉淀的pH |
8.9 |
1.5 |
完全沉淀的pH |
10.9 |
2.8 |
(6)结合流程中的数据计算。
①菱铁矿中镁元素的质量分数为 (不考虑整个流程转化中的损失)。
②MgCl2通电制得的气体的质量(写出计算过程)。
将适量二氧化碳通入100g氢氧化钠溶液中。恰好完全反应后,得到108.8g碳酸钠溶液请计算:
(1)参加反应的二氧化碳的质量为 g;
(2)氢氧化钠溶液的溶质质量分数。
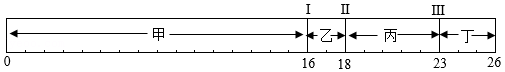
在一密闭容器中,有甲、乙、丙、丁四种物质,反应前各物质的质量关系如图刻度纸所示(例如:丙的质量为5g,丁的质量为3g),充分反应后,在同一张刻度纸上再次记录各物质的质量变化:刻度线Ⅰ向左移动16格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向左移动8格。下列说法正确的是( )
| A. |
该反应是化合反应 |
| B. |
丙一定是催化剂 |
| C. |
反应后丁的质量为8g |
| D. |
反应生成的乙和丁的质量比为1:1 |
某化学兴趣小组为了测定某纯碱样品(只含有Na2CO3、NaCl)中Na2CO3质量分数,取5克样品,往其中加入一定质量的稀盐酸,产生气体的质量与所加稀盐酸的质量变化如图,试计算:
(1)共产生 克二氧化碳;
(2)该纯碱样品中Na2CO3的质量分数;
(3)求恰好完全反应时所得溶液的质量分数?

我国塑料购物袋的年消耗量很大,废弃塑料的处理亟待解决。回答下列问题。
(1)购物袋等塑料制品的大量使用,可能会造成的一种环境污染是 。
(2)小林尝试用焚烧法对某类塑料购物袋(主要成分是聚氯乙烯)进行处理,并将燃烧产物用氢氧化钠溶液进行吸收。
【查阅资料】Ⅰ.聚氯乙烯的化学式为(C2H3Cl)n。
Ⅱ.氯化氢气体会污染环境
Ⅲ.Na2CO3+CaCl2═CaCO3↓+2NaCl
①聚氯乙烯完全燃烧的化学方程式如下:
2(C2H3Cl)n+5nO2 4nCO2+2nHCl+2nX,则X的化学式为 。
②将完全燃烧后的产物,全部通入到一定量的NaOH溶液中,得到吸收液,写出氢氧化钠溶液吸收氯化氢的化学方程式 。
③小林对吸收液的溶质成分产生了兴趣,进行如下探究:
[提出问题]吸收液中溶质的成分是什么?
[进行实验1]取吸收液少许置于试管中,滴加2~3滴无色酚酞试液,发现酚酞变红色,说明溶液呈 性。
[猜想]猜想1:NaCl、NaOH、Na2CO3
猜想2:
猜想3:NaCl、Na2CO3、NaHCO3
猜想4:NaCl、NaHCO3
[进行实验2]向实验1所得溶液中,加入过量的CaCl2溶液,小林观察到 (填实验现象),最终得出结论:猜想1正确。
[交流反思]实验结束后,小林对吸收液进行无害化处理,其方案是 ,然后倒入废液缸。
咨询老师后,小林获悉废弃塑料的资源化回收是减少环境危害的最好方法。
(3)聚氯乙烯的生产需要用到氯气。工业上获取氯气的方法是电解饱和食盐水,发生反应的化学方程式为:2NaCl+2H2O 2NaOH+H2↑+Cl2↑.某工厂需生产14.2t氯气(Cl2),至少需要氯化钠的质量为多少?(请写出计算过程)
孔雀石的主要成分是Cu2(OH)2CO3,还含有Fe2O3、Al2O3、SiO2杂质,用该矿石制备Cu的流程如图所示(部分产物略去):
 (1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(2)过程①中硫酸略过量,则过程②调pH除杂的最佳试剂是 (选填“CuO”或“Na2CO3”)。
(3)下列关于制取铜的两种方案的说法,正确的是 。
A.“方案一”得到的铜产品更纯
B.“方案一”不存在消耗能量的问题
C.“方案二”需考虑废气污染的问题
D.“方案二”得到纯铜的产率更高
(4)过程③发生的反应:2CuSO4+2H2O 2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
2020年9月,中国向世界宣布了2030年前实现碳达峰、2060年前实现碳中和的目标。
(1)为减缓大气中二氧化碳含量的增加,下列措施可行的是 (填序号)。
A.植树造林,开发和利用太阳能、水能、风能等新能源
B.禁止使用煤、石油、天然气等化石燃料
(2)绿色植物通过光合作用吸收二氧化碳,生成葡萄糖并放出氧气,其反应的化学方程式:6CO2+6H2O 葡萄糖+6O2,则葡萄糖的化学式为 。若吸收44g二氧化碳,理论上可释放出氧气 g。
葡萄糖+6O2,则葡萄糖的化学式为 。若吸收44g二氧化碳,理论上可释放出氧气 g。
(3)近年我国科学家合成了一种新型催化剂,可将二氧化碳和氢气转化为清洁的液体燃料甲醇(CH3OH)和水,该反应的化学方程式为 。
(4)将一氧化碳和二氧化碳的混合气体3.2g通过足量灼热氧化铜粉末,充分反应,将所得的气体全部通入足量的氢氧化钡溶液中,气体全部被吸收,生成白色碳酸钡沉淀,溶液质量减少15.3g。则原混合气体中碳、氧元素的质量比为 (填最简比)。
如图所示四个图像对应的变化过程正确的是( )
A. 气体物质的溶解度与温度和压强的关系
气体物质的溶解度与温度和压强的关系
B. 浓硫酸长时间露置于空气中
浓硫酸长时间露置于空气中
C.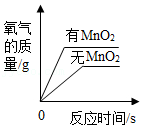 用等质量、等浓度的过氧化氢溶液分别制取氧气
用等质量、等浓度的过氧化氢溶液分别制取氧气
D.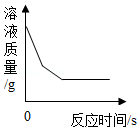 向足量的硫酸铜溶液中加入铁和镁固体混合物
向足量的硫酸铜溶液中加入铁和镁固体混合物
某工厂利用废铁屑与废硫酸反应制取绿矾(FeSO4•7H2O)。
(1)绿矾中铁原子与氧原子个数比为 。
(2)现有废硫酸4.9t(硫酸的质量分数为20%)与足量的废铁屑反应,理论上可生产出绿矾的质量是多少?(请写出计算过程,结果保留三位有效数字,下同)
(3)若配制100g质量分数为20%的稀硫酸溶液,需质量分数为98%的浓硫酸的体积是多少?(已知:质量分数为98%的浓硫酸的密度为1.84g/cm3)。