把干燥、纯净的氯酸钾和二氧化锰的混合物31.5g装入大试管中,加热制取氧气。待完全反应后,将试管冷却、称量,得到21.9g固体物质。计算制得氧气多少克?21.9g固体物质中含有哪些物质?各多少克?
将氯酸钾和二氧化锰的固体混合物20g加入试管中,加热。待完全反应后,将试管冷却、称量,试管内固体物质为15.2g。计算:
(1)反应生成的氧气质量为 g。
(2)列式计算原固体混合物中氯酸钾的质量。
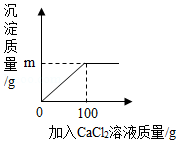
在一定温度下,向20gNa 2CO 3和NaCl的固体混合物中加入101g水,溶解后,再向其中加入100gCaCl 2溶液恰好完全反应,过滤,所得滤液的质量为211g,将滤渣洗涤、干燥,称其质量为m,试计算:
(1)m= g。
(2)当恰好完全反应时,所得溶液中溶质的质量分数为多少?
煤属于不可再生资源,将煤通过一定方式可转化为汽油、乙醇(C 2H 5OH)和气体燃料。乙醇可用作燃料。我国已经推广使用一种车用乙醇汽油,这种汽油的燃烧废气对环境的污染较少,请计算:
(1)69g乙醇完全燃烧,生成二氧化碳的质量为多少?(要求写出计算过程)
(2)在氧气不足的情况下,乙醇不完全燃烧生成一氧化碳、二氧化碳和水,若69g乙醇不完全燃烧生成88g二氧化碳,则反应生成一氧化碳和水的分子个数比为 。
氧气是人类生产活动的重要资源。
( 1 )下列属于 O 2 的化学性质的是 (填标号)。
| A. |
O 2能支持燃烧 |
| B. |
O 2的密度比空气的密度略大 |
| C. |
O 2在低温、高压时能变为液体或固体 |
( 2 )小圳同学进行实验室制备 O 2 的相关探究。
【 查阅 】 他得知在 KClO 3 分解制 O 2 的反应中, Fe 2 O 3 可作催化剂。
【 实验 】 他用电子秤称取 0.49g Fe 2 O 3 和一定量的 KClO 3 ,充分混合后加热至 KClO 3 完全分解,冷却至室温,称得剩余固体的质量为 1.98g 。
【计算】①剩余固体中KCl的质量是 g。
② 该反应生成 O 2 的质量(根据化学方程式写出完整的计算步骤)。
【 思考 】 他发现制备 O 2 较慢,猜测 KClO 3 和 Fe 2 O 3 的质量比可能会影响反应的快慢。
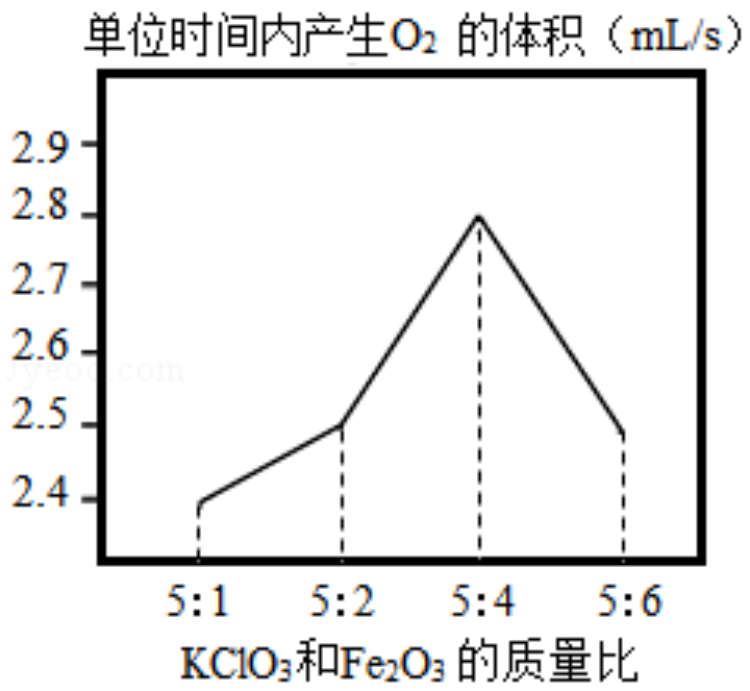
【 探究 】 ③ 他调节 KClO 3 和 Fe 2 O 3 的质量比制备 O 2 ,整理数据绘制出如图,从图中得出 KClO 3 和 Fe 2 O 3 最佳质量比是 。
【 结论 】 ④ 根据质量守恒定律,请你计算出小圳同学在 [ 实验 ] 中称取的 KClO 3 的质量为 g , KClO 3 和 Fe 2 O 3 的质量比是 (填最简比),不是最佳质量比。