如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )

A.a的溶解度大于b的溶解度
B.P点表示t1℃时a、c两物质溶解度相等
C.将t1℃饱和的c溶液升温到t2℃,得到的是不饱和溶液
D.将t2℃,a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数由大到小的顺序为:b>a=c
NaCl和KNO3在不同温度时的溶解度如下表。下列说法错误的是( )
温度/℃ |
0 |
20 |
40 |
60 |
NaCl的溶解度/g |
35.7 |
36.0 |
36.6 |
37.3 |
KNO3的溶解度/g |
13.3 |
31.6 |
63.9 |
110 |
A.20℃时,100g H2O最多能溶解36.0g NaCl
B.40℃时,KNO3饱和溶液的溶质质量分数小于63.9%
C.可用冷却海水的方法获取大量食盐
D.其他条件不变,升温可将KNO3饱和溶液变为不饱和溶液
不同温度下KNO3的溶解度如下表所示。下列说法正确的是( )
温度/℃ |
20 |
30 |
40 |
溶解度/g |
31.6 |
45.8 |
63.9 |
A.20℃时,100g KNO3饱和溶液中溶质质量为31.6g
B.30℃时,100g KNO3饱和溶液的溶质质量分数为45.8%
C.30℃时,将50g KNO3放入100g水中得到150g溶液
D.40℃时,100g水最多溶解63.9g KNO3
甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是( )

A.甲一定是不饱和溶液
B.丙和丁一定是饱和溶液
C.乙的溶质质量分数一定比甲大
D.甲和丙的溶质质量分数一定不相等
甲是60℃的蔗糖溶液,按如图所示进行操作。以下分析错误的是( )

A.甲一定是不饱和溶液
B.丙和丁一定是饱和溶液
C.乙的溶质质量分数一定比甲大
D.甲和丙的溶质质量分数一定不相等
如图所示为蒸发氯化钠溶液的过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态,分析实验过程,

可以作出的正确判断是( )
A.在①→②过程中,氯化钠的质量分数保持不变
B.在②→③过程中,氯化钠的溶解度不断增大
C.在③→④过程中,水的质量分数不断增大
D.在②→④过程中,氯化钠的质量分数先不变后增大
下列说法正确的是( )

A.水灭火的主要原理是水吸热降低了可燃物的着火点
B.用蒸馏的操作净化水不能降低水的硬度
C.根据如图可知,降温可使氢氧化钙饱和溶液变为不饱和溶液
D.20℃时,KCl的溶解度为34g,该温度下,100g KCl饱和溶液中溶质KCl的质量为34g
如图是化合物M和化合物N的溶解度曲线。下列说法中错误的是( )

A.30℃时,M和N的溶解度相等
B.将60℃时N的饱和溶液降温至40℃,有晶体析出
C.M的溶解度随温度的升高而增大
D.N的饱和溶液在40℃时溶质质量分数最大
如图是甲、乙、丙三种固体物质的溶解度曲线。下列说法错误的是( )

A.T2℃时,向各装有50g水的三个烧杯中,分别加入甲、乙、丙固体各40g,充分搅拌后形成饱和溶液的是乙和丙
B.甲中混有少量的乙,提纯甲的常用方法是降温结晶
C.在T1℃时,将接近饱和的丙溶液变为饱和溶液,溶剂的质量可能不变
D.将T2℃的甲、乙、丙饱和溶液温度降至T1℃,溶液中溶质的质量分数大小关系为乙=丙>甲
如图为甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线。下列相关说法中正确的是( )

A.甲和乙两物质的饱和溶液温度从t3℃降至t2℃时,析出晶体质量甲>乙
B.将接近饱和的丙溶液变为饱和溶液,可以采用升高溶液温度的方法
C.甲中含少量乙时,采用蒸发溶剂的方法提纯甲
D.t1℃时,30g丙物质加入到50g水中形成溶液的质量为80g
以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
0℃ |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
60℃ |
|
Na2CO3的溶解度(g/100g水) |
7.1 |
12.5 |
21.5 |
39.7 |
49.0 |
48.5 |
46.0 |
NaHCO3的溶解度(g/100g水) |
6.9 |
8.1 |
9.6 |
11.1 |
12.7 |
14.5 |
16.4 |
A.40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B.60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C.30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D.20℃的饱和Na2CO3溶液中通足量CO2,生成的 NaHCO3会部分析出
根据图示实验、部分记录和溶解度曲线,判断下列说法正确的是( )
A.无法判断a中溶液是否为饱和溶液
B.c中溶液溶质的质量分数为33.3%
C.b中溶液在加热过程中始终为饱和溶液
D.常用冷却热的饱和溶液的方法获得氯化钠晶体
T℃时,向盛有100g水的两烧杯中分别加入60g甲、乙两种固体,搅拌后固体甲完全溶解,放置一段时间后,甲溶液中有固体析出,溶解度曲线如图所示。下列说法正确的是( )
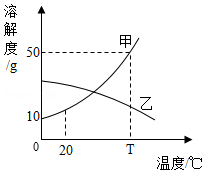
A.搅拌的目的是增大物质的溶解度
B.将T℃的甲、乙两种饱和溶液降温,溶质质量分数都减小
C.甲溶于水的过程中一定放出热量
D.乙是可溶性物质
如图是四种物质的溶解度曲线,下列说法中正确的是( )

| A. |
20℃时,分别配制四种物质的饱和溶液,硫酸铵需要水的质量最少 |
| B. |
40℃时,向硫酸铵饱和溶液中加入适量氯化钾固体会析出硫酸钾晶体 |
| C. |
氯化钾饱和溶液的溶质质量分数一定小于氯化铵饱和溶液的溶质质量分数 |
| D. |
用30克硫酸钾固体最多可配制150克80℃的硫酸钾饱和溶液 |