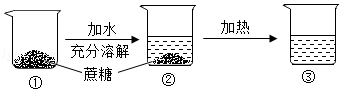
某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是( )
| A. |
②中溶液是饱和溶液 |
| B. |
③中溶液一定是不饱和溶液 |
| C. |
②③中溶液的溶质质量分数不相同 |
| D. |
③中溶液的溶质质量大于②中溶液的溶质质量 |
某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是( )
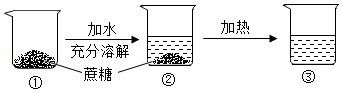
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
硫酸镁在工农业以及医疗上有广泛应用,其溶解度如表所示。则下列说法正确的是( )
温度/℃ |
10 |
30 |
50 |
70 |
90 |
溶解度/g |
27.7 |
39.3 |
49.0 |
54.1 |
51.1 |
A.硫酸镁的溶解度随温度升高而增大
B.10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液
C.50℃时,100g的硫酸镁饱和溶液中溶质和溶剂的质量比为49:100
D.70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数增大
如图为KNO3和NaCl的溶解度曲线,下列说法不正确的是( )

A.20℃时,KNO3的溶解度为31.6g
B.a点处KNO3和NaCl两种溶液中溶质的质量分数相等
C.40℃时,100g水中可溶解KNO3固体63.9g
D.0℃时,NaCl饱和溶液中溶质的质量分数为35.7%
现有一含NaCl杂质的Na2CO3样品,取13.9g样品溶于水,配成104.4g溶液,此溶液与100g某浓度的盐酸恰好完全反应,得到200g溶液。请计算:
(1)生成的二氧化碳的质量为 g;
(2)所得溶液中NaCl的质量分数(写出计算步骤)。
下列图象中有关量的变化趋势正确的是( )
A. 向一定浓度的NaOH溶液中加水稀释
向一定浓度的NaOH溶液中加水稀释
B. 向一定浓度的H2SO4溶液中加水稀释
向一定浓度的H2SO4溶液中加水稀释
C. 向一定质量的锌粒中加入稀盐酸
向一定质量的锌粒中加入稀盐酸
D.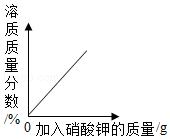 向接近饱和的KNO3溶液中加入KNO3晶体
向接近饱和的KNO3溶液中加入KNO3晶体
根据如图所示溶解度曲线判断,下列说法正确的是( )
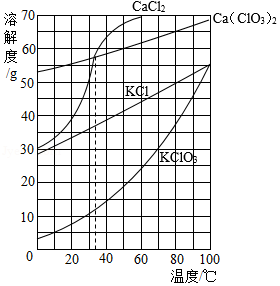
A.20℃时,将10 g KClO3加入100 g水中,溶液质量为110 g
B.30℃时,KCl饱和溶液中溶质的质量分数约为35%
C.分别将35℃的CaCl2和Ca(ClO3)2两种饱和溶液升温至40℃,CaCl2溶液中溶质的质量分数较大
D.除去CaCl2中混有的少量Ca(ClO3)2,可在较高温度配成饱和溶液,再降温结晶、过滤
甲、乙、丙三种物质的溶解度曲线如图所示。下列说法错误的是( )
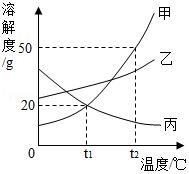
A.t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是:乙>甲=丙
B.t2℃时,30g甲物质加入50g水中,充分搅拌后,所得溶液的溶质的质量分数为37.5%
C.将相同质量的甲、乙、丙三种物质的饱和溶液从t2℃降温到t1℃,析出晶体最多的是甲
D.欲将丙物质的不饱和溶液变为饱和溶液,可以采取升高温度的方法
氯化钾(KCl)和氯酸钾(KClO3)的溶解度随温度变化曲线如图所示,下列说法正确的是 ( )

A.30℃时,KCl饱和溶液的溶质质量分数为35%
B.60℃时,a点对应KCl溶液恒温加水可变饱和
C.KCl的溶解度随温度变化的趋势比KClO3大
D.90℃150gKClO3饱和溶液降温到10℃可析出45g晶体
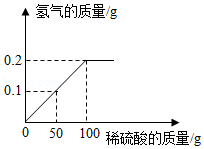
铜锌合金又称假黄金。向盛有30g铜锌合金粉末样品的烧杯中逐渐加入稀硫酸,生成氢气的质量与加入稀硫酸的质量关系如图所示,计算:
(1)充分反应后生成氢气的质量为 g。
(2)合金样品中锌的质量。
(3)恰好完全反应时,所得溶液溶质的质量分数。(结果保留一位小数)
为测定硫酸钠和硫酸镁固体混合物中硫酸镁的质量分数。某同学取固体混合物26.2g,向其中加入219.6g水,使其完全溶解配制成混合溶液。将200g一定溶质质量分数的氢氧化钠溶液平均分成5等份,依次加入到上述混合溶液中,生成沉淀的质量与加入氢氧化钠溶液的质量关系如下表:
| 次数 |
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
| 氢氧化钠溶液质量/g |
40 |
40 |
40 |
40 |
40 |
| 产生沉淀质量/g |
1.45 |
2.9 |
m |
5.8 |
5.8 |
试分析计算。
(1)m的值为 。
(2)固体混合物中硫酸镁的质量分数。(结果保留0.1%)
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数。