金属材料在日常生活、生产中有着广泛的运用,下列关于金属的说法不正确的是
| A.工业上金属Mg、Al都是用电解熔融的氯化物制得的 |
| B.合金的性质与其成分金属的性质不完全相同 |
| C.金属冶炼的本质是金属阳离子得到电子变成金属原子 |
| D.越活泼的金属越难冶炼 |
如表为某有机物与各种试剂的反应现象,则这种有机物可能是
| 试剂 |
钠 |
溴水 |
NaHCO3溶液 |
| 现象 |
放出气体 |
褪色 |
放出气体 |
A.CH2═CH﹣CH2﹣OH B.
C.CH2═CH﹣COOH D.CH3COOH
下列各组物质按如图所示转化关系每一步都能一步实现的是

| |
甲 |
乙 |
丙 |
丁 |
| A |
FeCl3 |
FeCl2 |
Fe2O3 |
Fe(OH)3 |
| B |
Cu |
CuO |
CuSO4 |
CuCl2 |
| C |
SO2 |
H2SO4 |
SO3 |
H2S |
| D |
Al(OH)3 |
NaAlO2 |
Al2O3 |
AlCl3 |
A.A B.B C.C D.D
乌洛托品在合成、医药、染料等工业中有广泛用途,其结构式如图所示.将甲醛水溶液与氨水混合蒸发可制得乌洛托品.若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为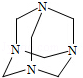
| A.1:1 | B.2:3 | C.3:2 | D.2:1 |
下列说法不正确的是
| A.为了提高生活用水的卫生标准,自来水厂常使用Cl2和FeSO4•7H2O进行消毒、净化,以改善水质 |
| B.硝酸、纯碱、醋酸钾和硅石分别属于酸、碱、盐和氧化物 |
C. 从分类的角度看,混合物、分散系、胶体的从属关系如图所示 |
| D.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X和Y组成原电池时,Y为电池的负极.X、Y、Z三种金属的活动性顺序为
| A.X>Y>Z | B.X>Z>Y | C.Y>X>Z | D.Y>Z>X |
W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:四种元素的电子层数之和为10,且它们分别属于连续的四个主族;四种元素的原子中半径最大的是X原子.下列说法正确的
| A.四种元素中有两种元素在第二周期 |
| B.W所在主族元素的原子次外层电子数可能为2或8,不可能为18 |
| C.X、Y、Z的最高价氧化物对应的水化物两两之间能反应 |
| D.工业上获得X、Y单质的方法主要是电解其熔融的氯化物 |
下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O2(g)═CO2(g);△H1 C(s)+ O2(g)═CO(g);△H2
O2(g)═CO(g);△H2
②S(s)+O2(g)═SO2(g);△H3 S(g)+O2(g)═SO2(g);△H4
③H2(g)+ O2(g)═H2O(l);△H5 2H2(g)+O2(g)═2H2O(l);△H6
O2(g)═H2O(l);△H5 2H2(g)+O2(g)═2H2O(l);△H6
④CaCO3(s)═CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)═Ca(OH)2(s);△H8.
| A.① | B.④ | C.②③④ | D.①②③ |
某盐的混合物中含有0.2mol/L Na+、0.4mol/L Mg2+、0.4mol/L Cl﹣,则SO42﹣为
| A.0.1 mol/L | B.0.2 mol/L | C.0.3 mol/L | D.0.4 mol/L |
根据原子结构及元素周期律的知识,下列推断正确的是
A.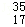 Cl2与 Cl2与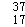 Cl2氧化能力相近,二者互为同位素 Cl2氧化能力相近,二者互为同位素 |
B.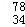 Se与 Se与 Se所含质子数相同,中子数不同 Se所含质子数相同,中子数不同 |
| C.同主族元素形成的含氧酸的酸性随核电荷数的增加而减弱 |
| D.同周期主族元素形成的简单离子半径随核电荷数的增大而减小 |
设NA为阿伏加德罗常数的数值.下列说法正确的是
| A.1mol甲苯含有6NA个C﹣H键 |
| B.18g H2O含有10NA个质子 |
| C.标准状况下,22.4L氨水含有NA个NH3分子 |
| D.56g铁片投入足量浓H2SO4中生成NA个SO2分子 |
关于室温下pH=3的醋酸和pH=3盐酸溶液,下列有关叙述正确的是( )
| A.二者水溶液中,水的电离程度相等 |
| B.均加水稀释10倍后,溶液的pH:醋酸>盐酸 |
| C.加水稀释,CH3COOH的电离程度在增大,溶液的导电能力在增强 |
| D.加入足量的Mg粉充分反应后,产生H2的体积V(相同状况):醋酸>盐酸 |
在恒容密闭容器中,NH3和NO在一定条件下发生如下反应:
2NH3(g) + NO(g) 2N2(g) + 3H2O(g) ΔH<0 下列有关说法正确的是( )
2N2(g) + 3H2O(g) ΔH<0 下列有关说法正确的是( )
| A.其它条件不变时,使用高效催化剂,不可以使NO的转化率增大 |
| B.平衡时,其它条件不变,充入NH3,平衡向右移动,NH3的转化率增大 |
| C.当混合气体的密度不变了,则反应达到化学平衡状态 |
| D.平衡时,其它条件不变,升高温度可使该反应的平衡常数增大 |
某同学设计了如图所示的盐桥式原电池,下列说法正确的是( )

| A.X若为Fe、Y可以为Na2SO4溶液 |
| B.X若为Cu、Y可以为AgNO3溶液 |
| C.电子由X电极经盐桥流向Ag电极 |
| D.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动 |
将0.1 mol AgNO3和0.2mol Cu(NO3)2固体溶于水配成100 mL溶液,用惰性电极电解一段时间后,在一极上析出0.15 mol O2,此时,另一极上析出的气体体积(标准状况)为( )
| A.1.12L | B.2.24 L | C.3.36 L | D.4.48L |