某同学在实验报告中记录下列数据,其中正确的是
| A.用25 mL量筒量取12.36 mL盐酸 | B.托盘天平称取8.75克食盐 |
| C.用酸式滴定管量取4.90mL硫酸 | D.用广泛pH试纸测得某溶液pH为3.5 |
用硫酸和铁屑制备硫酸亚铁,反应结束后,需将反应液进行过滤,但过滤时常出现漏斗颈下端管口堵塞的现象 ,可采取的措施是 ( )
,可采取的措施是 ( )
| A.将普通漏斗改为分液漏斗 | B.将漏斗预热,进行热过滤 |
| C.增加滤纸层数 | D.向溶液中加一些稀硫酸 |
下列说法正确的是
| A.可用碘水鉴别苯、四氯化碳、乙醇三种无色液体 |
| B.取11.7 g NaCl固体于烧杯中,加入200 mL蒸馏水(r=1g/cm3)充分搅拌可配成1mol/L的NaCl溶液 |
| C.测定溶液的酸碱性时,应先将pH试纸润湿,然后进行检测 |
| D.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应相等 |
下列实验中,所加物质的浓度不会影响实验现象的是 ( )
( )
A.向Fe(OH)3胶体中滴加HCl,先出现沉淀,后沉淀溶解 |
B.向少量苯酚溶液中滴入溴水,有白色沉淀产生 |
C.向盛有少量MnO2的烧瓶中加入盐酸,加热,有黄绿色气体产生 |
D.向盛有少量铜片的试管中加入H2SO4,加热,有气体放出 |
下表中实验“操作和现象”与“结论”对应关系正确的一组是
| |
操作和现象 |
结论 |
| A |
向纯碱中滴加足量浓盐酸,将产生的气体通入苯酚钠溶液,溶液变浑浊 |
酸性:盐酸>碳酸>苯酚 |
| B |
取某溶液少量,加入盐酸酸化的氯化钡溶液,出现白色沉淀 |
该溶液中一定含有大量的SO42- |
| C |
取少量Fe(NO3)2试样加水溶解,加稀硫酸酸化,滴加KSCN溶液,溶液变为红色 |
该Fe(NO3)2试样已经变质 |
| D |
在新制的银氨溶液试管中加入适量葡萄糖溶液,振荡、水浴加热,试管壁附着一层银白色金属 |
葡萄糖是还原性糖 |
下图甲是课本中验证铜和浓硝酸反应的装置,乙、丙是师生对演示实验改进后的装置:

(1)甲、乙、丙三个装置中共同发生反应的离子方程式是 。
(2)和甲装置相比,乙装置的优点是 。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。先关闭弹簧夹 ,再打开弹簧夹 ,才能使NO2气体充满试管②。
(4)当气体充满试管②后,将铜丝提起与溶液脱离,欲使烧杯中的水进人试管②,应进行的操作是 。
右图是一套检验气体性质的实验装置。向装置中缓慢地通入气体X,若关闭活塞K,则品红试液无变化,而澄清石灰水变浑浊;若打开活塞K,则品红试液褪色。据此判断气体X和洗气瓶内液体Y可能是( )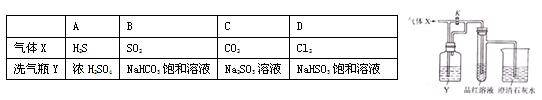
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是( )
A K+一定存在 B 100mL溶液中含0.01mol CO32-
C Cl-可能存在 D Ba2+一定不存在,Mg2+可能存在
以下离子检验的结论可靠的是( )
| A.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,说明有Ca2+ |
| B.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,说明有I- |
| C.往溶液中加入盐酸,产生的气体能使澄清石灰水变浑浊,说明有CO32— |
| D.往溶液中加入 BaC12溶液和稀 HNO3 ,有白色沉淀生成,说明有SO42- |
离子检验的常用方法有三种:
| 检验方法 |
沉淀法 |
显色法 |
气体法 |
| 含义 |
反应中有沉淀产生或溶解 |
反应中有颜色变化 |
反应中有气体产生 |
下列离子检验的方法不合理的是( )
A NH4+-气体法 B I--沉淀法 C Fe3+-显色法 D Ca2+-气体法