在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”。请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6 mol·L-1的盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。
图1 图2
填写下列空白:
(1)实验进行时试管A中应加入的试剂是;烧瓶B的作用是______________________;烧瓶C的作用是______________________;在试管D中收集得到的是
____________________________。
(2)实验时,U形管G中应加入的试剂是___________;长颈漏斗H中应加入___________。
(3)两套装置中,在实验时需要加热的仪器是(填该仪器对应的字母) ___________。
(4)烧瓶I中发生的反应有时要加入少量硫酸铜溶液,其目的是__________________________。
(5)试管E中发生反应的化学方程式是______________________________________________。
(6)为了安全,在E管中的反应发生前,在F出口处必须___________;E管中的反应开始后,在F出口处应___________。
(创新题)做一个家庭小实验:
(1)将蜡烛点燃,并燃烧几秒钟,等火焰稳定后,在其上方撒下小苏打粉末,火焰会出现什么现象?
(2)不慎将食盐水洒在煤气灶上,观察火焰的颜色。
解释上述两实验现象产生的原因。
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示的装置先进行了有关实验:

⑴B是用来收集实验中产生的装置,但未将导管画全,请将装置图补充完整。
⑵实验中他们取6.4g铜片和12mL 18mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①请写出铜与浓硫酸反应的化学方程式
②为什么有一定量的余酸但未能使铜片完全溶解?你认为原因是 。
③下列试剂中能够证明反应结束后的烧瓶中确有余酸的是 (填写字母编号)
| A.铁粉 | B.BaCl2溶液 | C.银粉 | D.Na2CO3溶液 |
(3)为了测定余酸的物质的量浓度,甲、乙两位同学进行了如下设计:
①甲同学设计方案是:
先测定铜与浓硫酸反应产生的SO2的量,再计算余酸的物质的量浓度,他认为测定SO2的量的方法有很多种,请问下列实验方案中不可行的是 (填写字母编号)
A:将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B:将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称量沉淀
C:用排水法测定装置A产生气体的体积(已折算成标准状况)
D:将装置A产生的气体缓缓通入足量的氢氧化钡溶液(预先除去了溶解O2),反应完全后,过滤、洗涤、干燥,称量沉淀(隔绝空气条件下)
②乙同学设计的方案是:
在反应后的溶液中加蒸馏水稀释至1000mL,取20mL于锥形瓶中,滴加2~3滴甲基橙指示剂,用标准氢氧化钠溶液进行滴定(已知:Cu(OH)2开始沉淀的pH约为5),通过测定出消耗NaOH溶液的体积来求余酸的物质的量浓度。假定反应前后烧瓶中溶液体积不变,你认为乙同学设计的实验方案能否求得余酸的物质的量浓度 ,(填能或否),其理由是 。
(4)请你再设计一个可行的实验方案来测定余酸的物质的量浓度。简要写出操作步骤及需要测定的数据,并写出相应的计算式。
有机物的C、H含量常用燃烧和与CuO灼烧等方法使之生成 和水,测它们的质量求得有机物中碳和氢的百分含量,现有某固态有机物在加热情况下鼓入足量的氧气使其完全燃烧,今有如下仪器。
和水,测它们的质量求得有机物中碳和氢的百分含量,现有某固态有机物在加热情况下鼓入足量的氧气使其完全燃烧,今有如下仪器。
(1)为确定某固体有机物的最简式(实验式)下述仪器中最少需要的种类有________种,它们是________,其中要一前一后用两次的是________,(填仪器编号)其作用前者为________;后者为________。但为完成测定还缺少的一种重要仪器名称是________。
(2)为确定固体有机物是烃还是其含氧衍生物,实验依据是________.
(3)为确定其分子式还需知道下述中的
A. 熔、沸点 B. 定温、定压下蒸气密度
C. 固定有机物的体积 D. 重要的化学性质
某校课外实验小组进行铜与浓、稀硝酸反应的实验研究。基本原则是:安全可靠、现象明显,符合环保要求。
如果用图Ⅰ中装置进行铜与浓硝酸反应的实验,最大缺点是产生的NO2气体逸出污染空气;如果用该装置来证明铜与稀硝酸反应生成NO气体,缺点是不易观察到有毒性的NO气体无色的本来面目。
(1)若用装置Ⅱ进行实验,既可克服实验不足,还能使上述反应在同一试管中连续进行。实验如下:组装好装置并检查气密性后,加入2 mL浓硝酸(铜片未接触酸液),塞紧胶塞;向左倾斜试管使其反应发生,当导管口有极少量红棕色气体逸出,溶液呈绿色时,正立试管,使反应停止;同时将导管插入水中,稍后能观察到:a.水沿导管倒吸至试管中,b.________________,c. ________________等明显现象。其中发生的原因用方程式表示为:_________________________________________________________。
(2)当试管中液体体积约占1/2时,从水中取出导管,并伸入一小试管中,管口塞上浸有碱液的棉花(如图Ⅲ)。这样做的目的是:________________,此时大试管中反应的离子方程式为:________________________________________________。
(3)若用右上图Ⅳ所示的装置(U形管、干燥管、A为活塞)制取NO可能更加理想。请补充下列实验步骤:
①检查装置的气密性的方法是:________________________________________________。
②打开活塞A,从U形管右端注入稀硝酸,直到________________________为止。
③关闭活塞A,若反应缓慢,可在U形管左侧加热,观察到____________________。
某品牌消毒液包装说明的部分内容摘录如下:主要有效成份为次氯酸钠,有效氯含量8000-10000mg/L。可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用。切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品。本品须密封,置阴凉暗处保存。请完成以下实验探究过程:
1.阅读材料,获取信息
⑴推测该消毒液的酸碱性: ,原因是(用离子方程式表示) 。
⑵该消毒液还具有的化学性质是 性和 性。
⑶从该消毒液的保存要求分析,导致其失效的外界因素主要是 。
2.确定要研究的问题
该消毒液对碳钢制品是否有腐蚀作用?
3.设计方案,实施探究
用烧杯取少量样品,将一颗光亮的铁钉放入烧杯,浸泡一段时间。对可能产生的现象有如下假设:
假设①:有明显现象;假设②:无明显现象。
⑷基于假设①,结论是铁钉被腐蚀,预期的实验现象是 。
⑸基于假设②,结论是 ,请设计实验进一步验证该结论,叙述实验操作: 。

(1) 实验过程中,可能观察到的主要现象有:
① ;
② ;
③ ;
④ ;
(2) 用该装置做铜与浓硝酸反应的实验,最突出的优点是 。
(3) 若要验证最终得到的气体生成物,最简便的方法是 。
铁生锈是比较常见的现象,某实验小组,为研究铁生锈的条件,设计了以下快速、易行的方法:
图11-21
首先检查制氧装置的气密性,然后按图11-21连接好装置,点燃酒精灯给药品加热,持续3分钟左右,观察到的实验现象为:①直形管中用蒸馏水浸过的光亮铁丝表面颜色变得灰暗,发生锈蚀;②直形管中干燥的铁丝表面依然光亮,没有发生锈蚀;③烧杯中潮湿的铁丝表面依然光亮。
试回答以下问题:
(1)由于与金属接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于_________。能表示其原理的反应方程式为___________________________。
(2)仪器A的名称为_________,其中装的药品可以是_________,其作用是_________。
(3)由实验可知,该类铁生锈的条件为_________。决定铁生锈快慢的一个重要因素是_________。
全世界每年因生锈损失的钢铁约占世界钢铁年产量的1/4。某学生想探究铁生锈的条件,他将干净的铁钉分别同时放入A、B、C三支试管中进行研究。
(1)请你帮助该学生完成下列实验设计的内容:
| 编号 |
操作方法 |
实验目的 |
| A |
|
探究铁在干燥空气中的生锈情况 |
| B |
放入铁钉,注入蒸馏水浸没铁钉,并用植物油液封 |
|
| C |
|
探究铁在有空气和水封时的生锈情况 |
(2)一周后,编号为___________的试管中的铁钉最易生锈。
(3)用相同材料制作,经过相同时间防锈处理的铁栏杆,安装在南方比安装在北方更易生锈,其原因是_____________________________________________。
(4)在焊接铁管时,为了使接口更加牢固,常用稀盐酸清洗接口处的铁锈,该反应的化学方程式为_______________________________________________。
(13分)下面是某学校研究化学反应中能量变化情况的实验:(氢氧化钡晶体与氯化铵晶体的反应)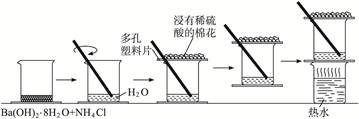
下表是某学生根据上述实验方案和步骤列表整理的实验事实和结论:
| 实验步骤 |
实验现象 |
得出结论 |
| 将晶体混合后立即用玻璃棒快速搅拌混合物 |
有刺激性气味的气体产生,该气体能使湿润的紫色石蕊试纸变蓝 |
|
| 用手触摸烧杯下部 |
感觉烧杯变凉 |
|
| 用手拿起烧杯 |
烧杯下面的带有几滴水的玻璃片(或小木板)粘到了烧杯底部 |
|
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上一会儿再拿起 |
玻璃片脱离上面烧杯底部 |
|
| 反应完后移走烧杯上的多孔塑料Q片,观察反应物 |
混合物成糊状 |
|
(1)请你根据实验现象得出相应的实验结论填入上表中。
(2)用化学方程式表示上述反应为_________________________________________________。
2001年6月21日,河南的郑州、洛阳及南阳市率先使部分汽车采用封闭运行方式,试用新的汽车燃料——车用乙醇汽油。乙醇,俗名酒精,它是以玉米、小麦、薯类等为原料经发酵、蒸馏而制成的。乙醇进一步脱水,再加上适量汽油后形成变性燃料乙醇。而车用乙醇汽油就是把变性燃料乙醇和汽油按一定比例混配形成的车用燃料。结合有关知识,完成以下问题:
(1)乙醇的结构简式为_____________。汽油是由石油分馏所得的低沸点烷烃,其分子中的碳原子数一般在C5—C11范围内,如戊烷,其分子式为__________________,结构简式及其同分异构体分别为_____________、_____________、_____________。
(2)乙醇可由含淀粉〔(C6H10O5)n〕的农产品,如玉米、小麦、薯类等经发酵、蒸馏而得。请写出由淀粉制乙醇的化学方程式:
①淀粉+水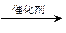 葡萄糖(C6H12O6)
葡萄糖(C6H12O6)
②葡萄糖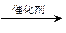 乙醇
乙醇
(3)淀粉可由绿色植物经光合作用等一系列生物化学反应得到,即水和二氧化碳经光合作用生成葡萄糖,由葡萄糖再生成淀粉。进行光合作用的场所是_____________,发生光合作用生成葡萄糖的化学方程式是
__________________________________________________________。
(4)乙醇充分燃烧的产物为__________________和__________________。
(5)车用乙醇汽油称为环保燃料,其原因是__________________________________________。
可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)请填空: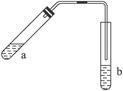
(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序的操作是________________________________________。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是__________________。
(3)实验中加热试管的目的是:
①____________________________________________________________________________。
②____________________________________________________________________________。
(4)试管b中加有饱和Na2CO3溶液,其作用是_________________________________________
______________________________________________________________________________。
(5)反应结束后,振荡试管b静置,观察到的现象是_________________________________
_______________________________________________________________________________
(9分)同学们已经学习了几种典型的有机化学反应类型——取代反应、加成反应、酯化反应,写出下列反应的化学反应方程式,并判断其反应类型。
(1)由乙烯制氯乙烷:____________________________,属于______________反应。
(2)由苯制取硝基苯:____________________________,属于______________反应。
(3)由苯制取环己烷:____________________________,属于______________反应。
(12分)温度对化学反应速率影响的实验探究根据下图所给出的仪器和药品进行实验。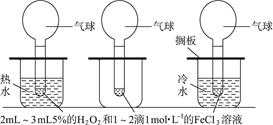
操作方法:在三支相同的试管中分别加入2 mL—3 mL约5%的H2O2,然后在每支试管中滴加2滴1 mol·L-1的FeCl3溶液后立即套上气球(大小相同)。等三支试管上的气球大小差不多相同时,同时置于三个烧杯中观察现象。
实验现象为___________________________________________________________________。
实验结论为___________________________________________________________________。