某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按下图所示转化进行综合利用。其中B是A水解的最终产物;C的化学式为C3H6O3,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色。(图中部分反应条件及产物没有列出)
(1)写出下列物质的结构简式:
①高分子化合物F_________________;②C脱水生成的六元环状化合物的结构简式___________。
(2)写出反应G→H的化学方程式: 。
(3)写出A与浓硝酸在一定条件下的反应 ,该反应类型为 。
某地市场销售的某种食用精制盐包装袋上有如下说明:
| 产品标准 |
GB5461 |
| 产品等级 |
一级 |
| 配 料 |
食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) |
20~50mg/kg |
| 分装时期 |
|
| 分装企业 |
|
⑴碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
⑵上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是 。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是 。
⑶已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a. 准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液10.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是 。
②b中反应所产生的I2的物质的量是 mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是 (以含w的代数式表示) _________________________mg/kg。
己知Zn跟一定量的浓H2SO4反应生成的气体产物有2种;请从下图中选用所需的仪器组成一套进行该反应并检出气体产物的装置(装置可重复选用,假设每步反应都进行的完全,且无需干燥)。现提供Zn、浓H2SO4、其它试剂自选(固定仪器用的铁夹、铁架台及加热装置等均略去)。将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加的试剂、作用及现象。(可不填满, 也可加行)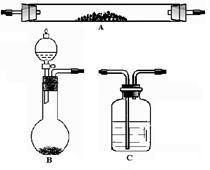
| 选用的仪器 (填字母) |
加入的试剂 |
作用 |
现象 |
| |
Zn、 浓H2SO4、 |
产生2种气体 |
/ |
| |
|
|
|
| |
|
除SO2 |
/ |
| |
|
|
|
| |
|
|
|
某试剂厂用银(含杂质铜)和硝酸(含杂质Fe3+)反应制取硝酸银。步骤如下:
根据上述步骤,完成下列填空:
(1)溶解银的硝酸应该用______硝酸(填浓或稀)原因是______
(a)减少过程中产生NOx的量(b)减少原料银的消耗量(c)节省硝酸的用量
(2)步骤B加热保温的作用是______
(a)有利于加快反应速度 (b)有利于未反应的硝酸挥发 (c)有利于硝酸充分反应,降低溶液中[H+]
(3)步骤c是为了除去Fe3+、Cu2+等杂质,冲稀静置时发生的化学反应是______;
(a)置换反应 (b)水解反应 (c)氧化——还原反应产生的沉淀物化学式:______