常温下,下列说法不正确的是
| A.0.1 mol/L的Na2SO3溶液中粒子浓度关系:c(OH-)=c(HSO3-)+2c(H2SO3)+c(H+) |
| B.将常温下pH=12的氢氧化钠溶液与pH=2的醋酸溶液等体积混合后,溶液呈碱性 |
| C.把等体积的1×10-5 mol/L的硫酸与4×10-5 mol/L的NaOH溶液相混合,混合液的pH值与5×10-6 mol/L的Ba(OH)2溶液的pH值相同 |
| D.0.2 mol·L-1CH3COOH溶液与0.1 mol·L-1NaOH溶液等体积混合:2c(H+)-2c(OH-) = c(CH3COO-)-c(CH3COOH) |
下列说法或解释不正确的是
| A.等物质的量浓度的下列溶液中,①NH4Al(SO4)2 ②NH4Cl ③CH3COONH4④NH3·H2O,c(NH4+)由大到小的顺序是①>②>③>④ |
| B.室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42—)>c(NH4+)>c(OH-)=c(H+) |
| C.向0.2 mol·L-1 NaHCO3溶液中加入等体积0.1 mol·L-1 NaOH溶液:c(CO32—)>c(HCO3—)>c(OH-)>c(H+) |
| D.物质的量浓度均为1 mol·L-1的NaCl和MgCl2混合液1 L中,含有Cl-的数目为3NA(NA表示阿伏加德罗常数的值)) |
25℃时将pH=3的强酸与pH=12的强碱溶液混合,所得溶液pH=10,则强酸与强碱的体积比是
| A.1︰9 | B.9︰1 | C.1︰11 | D.11︰1 |
有①CH3COOH、②HCl、③H2SO4三种溶液,下列说法不正确的是
| A.pH相同时,其物质的量浓度由大到小的顺序是①>②>③ |
| B.物质的量浓度相同时,其pH由大到小的顺序是①>②>③ |
| C.中和等量的烧碱溶液,需等物质的量浓度的①②③三种酸溶液的体积比为2∶2∶1 |
| D.体积和物质的量浓度均相同的①②③三溶液 ,分别与同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积比为2∶1∶2 |
将0.l mol· 氨水溶液加水稀释,下列说法正确的是
氨水溶液加水稀释,下列说法正确的是
| A.溶液中c(H+)和c(OH-)都减小 | B.溶液中c(OH-)增大 |
| C.NH3·H2O电离平衡向左移动 | D.溶液的pH减小 |
常温下,用0.1000 mol·L-1NaOH溶液滴定20.00 mL 0.1000 mol·L-1CH3COOH溶液所得滴定曲线如下图。下列说法正确的是( )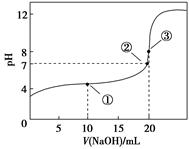
| A.点①所示溶液中: c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) |
| B.点②所示溶液中: c(Na+)=c(CH3COOH)+c(CH3COO-) |
| C.点③所示溶液中: c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| D.滴定过程中可能出现: |
c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
常温下,一定量的醋酸与氢氧化钠发生中和反应,当溶液中( )
| A.c(CH3COO-)=c(Na+)时,该溶液一定呈中性 |
| B.c(CH3COO-)=c(Na+)时,醋酸和氢氧化钠恰好完全中和 |
| C.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,可能是醋酸过量 |
| D.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,一定是NaOH过量 |
在一支25 mL的酸式滴定管中盛入0.1 mol·L-1HCl溶液,其液面恰好在5 mL的刻度处,若滴定管中的溶液全部放入烧杯中,然后用0.1 mol·L-1NaOH溶液进行中和,则需NaOH溶液的体积( )
| A.大于20 mL | B.小于20 mL |
| C.等于20 mL | D.等于5 mL |
若以w1和w2分别表示浓度为c1mol/L和c2mol/L硫酸的质量分数,已知2 w1=w2,则下列推断正确的是(硫酸的密度比纯水的大)
| A.2c1=c2 | B.2c2=c1 | C.c2>2c1 | D.c1<c2<2c1 |
常温下,0.1 mol·L-1氨水溶液中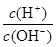 =1×10-8,下列叙述错误的是
=1×10-8,下列叙述错误的是
| A.该溶液中氢离子的浓度:c(H+ ) = 1×10-9 mol·L-1 |
| B.0.1 mol·L-1 氨水溶液与0.1 mol·L-1 HCl溶液等体积混合后所得溶液中: c(NH4+ ) + c(H+ ) = c(Cl- ) + c(OH-) |
| C.0.1 mol·L-1 的氨水溶液与0.05 mol·L-1 H2SO4溶液等体积混合后所得溶液中: c(NH4+ ) + c(NH3) + c(NH3·H2O) = 2c(SO42—) |
| D.浓度均为0.1mol·L-1 的NH3·H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则 |
c(NH4+ )>c(NH3·H2O)>c(Cl—)>c(OH-)>c(H+ )
中和相同体积、相同pH的H2SO4、HCl、CH3COOH三种溶液,所用相同浓度的NaOH的体积分别是V1、V2、V3,则三者的关系是:
| A.V1=V2=V3 | B.V1>V2>V3 | C.V3>V1>V2 | D.V1=V2<V3 |
把aL含硫酸铵和硝酸铵的混合液分成2等份,一份需用bmol烧碱刚好把铵全部赶出,另一份与氯化钡溶液反应时,消耗c mol氯化钡,由此可知原溶液中NO3-离子的物质量浓度为(单位:mol·L-1) ( )
| A.(2b-4c)/a | B.(b-2c)/a | C.(2b-2c)/a | D.(2b-c)/a |