一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”。如2Fe3+ + Cu ==2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e- ==Cu2+,还原反应式:2Fe3+ + 2e- ="=" 2Fe2+。并由此实现了化学能与电能的相互转化。据此,回答下列问题:
(1)将反应Zn + 2H+ = Zn2+ + H2↑拆写为两个“半反应式”:其中,氧化反应为: 。
(2)由题(1)反应,设计成原电池如图所示:
若电极a为Zn ,电极b可选择材料: (只填一种);电解质溶液甲是 ;电极b处的电极反应式: 。
(3)由反应2H2 + O2 2H2O ,设计出以稀硫酸为电解质溶液的燃料电池,其电极反应式为:负极 ,正极 。
2H2O ,设计出以稀硫酸为电解质溶液的燃料电池,其电极反应式为:负极 ,正极 。
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为4Al+3O2+6H2O=4Al(OH)3。下列说法不正确的是
| A.正极反应式为O2+2H2O+4e一=4OH— |
| B.以网状的铂为正极,可增大与氧气的接触面积 |
| C.电池工作时,电流由铝电极沿导线流向铂电极 |
| D.该电池通常只需更换铝板就可继续使用 |
甲醇是一种优质燃料,可制作燃料电池。
(1)工业上可用下列两种反应制备甲醇:
CO(g) + 2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
已知:2H2(g)+ O2(g) = 2H2O(g) ΔH3。则2CO(g)+O2(g) = 2CO2(g) 的反应热
ΔH=_____________(用ΔH1、ΔH2、ΔH3表示)。
(2)生产甲醇的原料CO和H2来源于:CH4(g) + H2O(g)  CO(g) + 3H2(g) ΔH4。
CO(g) + 3H2(g) ΔH4。
一定条件下CH4的平衡转化率与温度、压强的关系如图a。则ΔH4______0,P1_________P2
(填“<”、“>”或“=”)
(3)某实验小组设计如图b所示的甲醇燃料电池装置,工作一段时间后,溶液的PH (填增大、减小、不变)。负极的电极反应式为_______ ______。
(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制。粗铜电解得到精铜的的电解池中,阳极材料是 ;阴极材料是 ;
阳极泥为:
新型NaBH4/H2O2燃料电池(DBFC)的结构如图所示,(已知硼氢化钠中氢为-1价),有关该电池的说法正确的是
A.电极B材料中含MnO2层,MnO2可增强导电性
B.电池负极区的电极反应:BH4-+8OH--8e-→BO2-+6H2O
C.放电过程中,Na+从正极区向负极区迁移
D.在电池反应中,每消耗1L6mol/LH2O2溶液,理论上流过电路中的电子为6NA个
甲醇(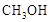 )是重要的能源物质,研究甲醇具有重要意义。
)是重要的能源物质,研究甲醇具有重要意义。
(1)利用工业废气中的 可制取甲醇,其反应为:
可制取甲醇,其反应为:
常温常压下已知下列反应的能量变化如图所示:
写出由二氧化碳和氢气制备甲醇的热化学方程式:
。
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了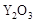 的
的  晶体,在高温下它能传导
晶体,在高温下它能传导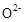 离子。电池工作时正极反应为 。
离子。电池工作时正极反应为 。
若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的物质的量为 mol。
(3)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后将 氧化成
氧化成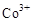 ,然后以
,然后以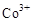 做氧化剂把水中的甲醇氧化成
做氧化剂把水中的甲醇氧化成 而净化。实验室用下图装置模拟上述过程:
而净化。实验室用下图装置模拟上述过程:
①写出阳极电极反应式 ;
②除去甲醇的离子反应为: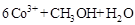
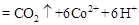 ,该过程中被氧化的元素是 ,当产生标准状况下2.24L
,该过程中被氧化的元素是 ,当产生标准状况下2.24L 时,共转移电子 mol。
时,共转移电子 mol。
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH + 3O2 + 4OH— =2CO32— + 6H2O,则下列说法错误的是
| A.放电时CH3OH参与反应的电极为正极 |
| B.充电时电解质溶液的pH逐渐增大 |
| C.放电时负极的电极反应为:CH3OH-6e-+8OH- = CO32— + 6H2O |
| D.充电时每生成1 mol CH3OH转移6 mol电子 |
全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的 材料,电池反应为: 。下列说法错误的是( )
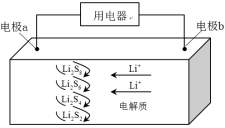
| A. |
电池工作时,正极可发生反应: |
| B. |
电池工作时,外电路中流过 电子,负极材料减重 |
| C. |
石墨烯的作用主要是提高电极a的导电性 |
| D. |
电池充电时间越长,电池中 的量越多 |
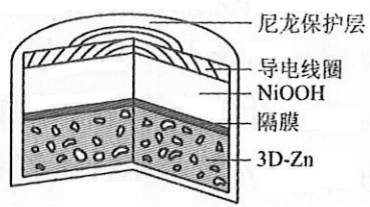
为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D−Zn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3D−Zn-NiOOH二次电池,结构如下图所示。电池反应为
。下列说法错误的是( )
| A. |
三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高 |
| B. |
充电时阳极反应为 |
| C. |
放电时负极反应为 |
| D. |
放电过程中 通过隔膜从负极区移向正极区 |
利用生物燃料电池原理研究室温下氨的合成,电池工作时
在电极与酶之间传递电子,示意图如下所示。下列说法错误的是( )

A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.阴极区,在氢化酶作用下发生反应
C.正极区,固氮酶为催化剂, 发生还原反应生成
D.电池工作时质子通过交换膜由负极区向正极区移动
如图为某种甲醇燃料电池示意图,工作时电子移动方向如图所示,下列判断正确的是( )

| A.X为氧气 |
| B.电极A反应式:CH3OH-6e-+H2O=CO2+6H+ |
| C.B电极附近溶液pH增大 |
| D.电极材料活泼性:A>B |
已知蓄电池在充电时作电解池,放电时作原电池,铅蓄电池上的两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”,关于标有“+”的接线柱,下列说法中正确的是
| A.充电时作阳极,放电时作负极 |
| B.充电时作阳极,放电时作正极 |
| C.充电时作阴极,放电时作负极 |
| D.充电时作阴极,放电时放正极 |
正、负极都是碳材料的双碳性电池,电池充、放电过程为2nC+LiA  CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是
CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是
| A.a是电池的负极 |
| B.放电时,A-离子向b极移动 |
| C.放电时,负极的电极反应式是nC-e-+A-= CnA |
| D.充电时,电解质中的离子浓度保持不变 |
下列生活中的化学事例对应的离子方程式书写正确的是
| A.用醋酸除去暖瓶中的水垢:2H++CaCO3="=" Ca2++ CO2↑+ H2O |
B.利用Na2CO3溶液可除油污:CO32- + 2H2O  H2CO3 + 2OH- H2CO3 + 2OH- |
| C.氢氧燃料电池在酸性介质中的正极反应:O2 +4e- +2H2O = 4OH- |
| D.汽车用的铅蓄电池充电时阳极反应:PbSO4+2H2O-2e-="=" PbO2+4H++SO42- |