分类、类比是学习化学常用的方法。
(1)在初中化学学习中,我们进行了比较物质的含量多少、测定物质的含量等不同类型的化学实验,据此将下列实验中的A与 分为一类,分类依据是 。 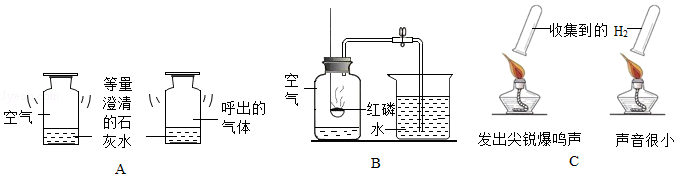
(2)CO+CuO Cu+CO 2 C+2CuO 2Cu+CO 2↑
在这两个反应中,一氧化碳和木炭都体现了还原性,其作用是 ;其中铜元素的化合价都是由 价变为0。
分类、类比是学习化学常用的方法。
(1)在初中化学学习中,我们进行了比较物质的含量多少、测定物质的含量等不同类型的化学实验,据此将下列实验中的A与 分为一类,分类依据是 。 
(2)CO+CuO Cu+CO 2 C+2CuO 2Cu+CO 2↑
在这两个反应中,一氧化碳和木炭都体现了还原性,其作用是 ;其中铜元素的化合价都是由 价变为0。