小明同学在课外阅读中得知:钠是一种活泼金属,常温下能与氧气,水发生反应,其中钠与水反应的化学方程式为:2Na+2H2O═2NaOH+H2↑,在实验室,该同学选取50ml一定溶质质量分数的硫酸铜溶液于烧杯中,再取绿豆大小的钠投入硫酸铜溶液中,充分反应后过滤,得到滤液和蓝色滤渣,并对滤液的成分进行探究。
[提出问题]滤液中溶质的成分是什么?
[查阅资料]已知Na2SO4的水溶液呈中性。
[猜想与假设]
猜想一:Na2SO4;
猜想二: ;
猜想三:Na2SO4、CuSO4;
猜想四:Na2SO4、CuSO4、NaOH;
其中不合理的是 ;
[实验方案与验证]
实验 |
实验操作 |
实验现象 |
实验结论 |
实验一 |
取少量滤液于试管中,观察现象 |
溶液为无色 |
猜想 成立 |
实验二 |
另取少量滤液于试管中,向其中滴加酚酞试剂 |
无明显现象 |
猜想 成立 |
实验三 |
常温下,再取少量滤液,测溶液酸碱度 |
pH=7 |
猜想 成立 |
[拓展延伸]金属钠在运输、保存中应该注意 。


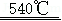 MgO+CO2↑
MgO+CO2↑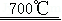 CaO+CO2↑
CaO+CO2↑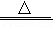 MgSO4+2NH3↑+H2O
MgSO4+2NH3↑+H2O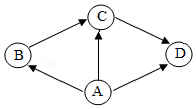

 粤公网安备 44130202000953号
粤公网安备 44130202000953号