为探究酸的性质,同学们设计了如下实验,请你参与。
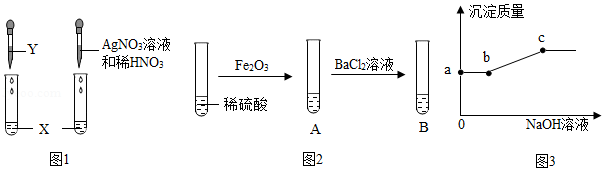
检验物质。按图1实验,可确定X是盐酸,则Y可以是 。
(1)确定溶质成分。由图2实验,A中固体全部溶解,B中有白色沉淀产生,得出结论:A中溶质只有硫酸铁。有同学认为该结论不合理。接着向试管B中滴加氢氧化钠溶液,且产生沉淀的量随氢氧化钠溶液量的关系如图3所示。则:A中溶质有 。实验中,A中发生反应的化学方程式为 ;a~b段对应溶液中一定发生反应的化学方程式为 ;c点对应溶液中含有溶质可能的组成有 。
(2)由以上实验总结酸的化学性质有 。
为探究酸的性质,同学们设计了如下实验,请你参与。

检验物质。按图1实验,可确定X是盐酸,则Y可以是 。
(1)确定溶质成分。由图2实验,A中固体全部溶解,B中有白色沉淀产生,得出结论:A中溶质只有硫酸铁。有同学认为该结论不合理。接着向试管B中滴加氢氧化钠溶液,且产生沉淀的量随氢氧化钠溶液量的关系如图3所示。则:A中溶质有 。实验中,A中发生反应的化学方程式为 ;a~b段对应溶液中一定发生反应的化学方程式为 ;c点对应溶液中含有溶质可能的组成有 。
(2)由以上实验总结酸的化学性质有 。