请根据下列装置回答问题。
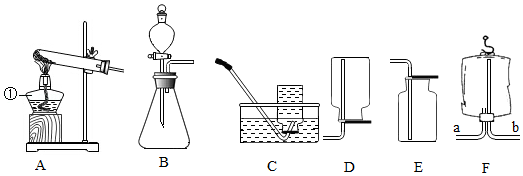
(1)写出A图中标号①的仪器名称 。
(2)用过氧化氢溶液和二氧化锰制取氧气。选择的发生装置是 (填装置序号);现准备收集一瓶氧气供铁丝燃烧的实验使用,选择 (填装置序号)装置收集氧气便于直接做这个实验;
(3)某同学利用空塑料输液袋(如图F)收集二氧化碳,验满二氧化碳时,把燃着的火柴放在玻璃管 (填“a”或“b”)端,如果火焰熄火。则收集满了。
请根据下列装置回答问题。

(1)写出A图中标号①的仪器名称 。
(2)用过氧化氢溶液和二氧化锰制取氧气。选择的发生装置是 (填装置序号);现准备收集一瓶氧气供铁丝燃烧的实验使用,选择 (填装置序号)装置收集氧气便于直接做这个实验;
(3)某同学利用空塑料输液袋(如图F)收集二氧化碳,验满二氧化碳时,把燃着的火柴放在玻璃管 (填“a”或“b”)端,如果火焰熄火。则收集满了。