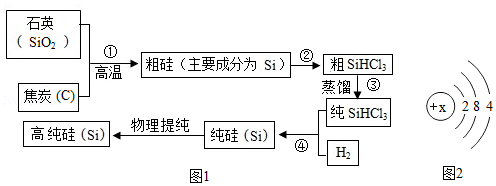
制作电脑芯片的材料为高纯硅,工业上制造高纯硅的基本流程如图1所示(某些反应过程中的部分物质没有在图中标出):
(1)SiHCl3中Cl元素的化合价为﹣1价,则Si元素的化合价为 。
(2)硅原子的结构示意图如图2所示,硅原子的核电荷数为 。
(3)第①步至第④步的变化中,属于物理变化的是第 步。
(4)第④步反应,除生成纯硅以外,还有HCl生成。写出第④步反应的化学方程式 。
制作电脑芯片的材料为高纯硅,工业上制造高纯硅的基本流程如图1所示(某些反应过程中的部分物质没有在图中标出):

(1)SiHCl3中Cl元素的化合价为﹣1价,则Si元素的化合价为 。
(2)硅原子的结构示意图如图2所示,硅原子的核电荷数为 。
(3)第①步至第④步的变化中,属于物理变化的是第 步。
(4)第④步反应,除生成纯硅以外,还有HCl生成。写出第④步反应的化学方程式 。