工业合成氨的反应为N2(g)+3H2(g)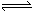 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应经过20分钟在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应经过20分钟在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为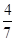 计算:
计算:
(1)H2在20分钟内的平均反应速率为 ;
(2)该条件下N2的平衡转化率为 ;(小数点后保留一位)
(3)该条件下反应2NH3(g)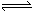 N2(g)+3H2(g)的平衡常数为 。(不带单位)
N2(g)+3H2(g)的平衡常数为 。(不带单位)


 H2O(g)+CO(g)△H<0,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。(已知此温度下该反应的平衡常数K=
H2O(g)+CO(g)△H<0,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。(已知此温度下该反应的平衡常数K= )
)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号