用系统命名法命名或写出结构简式:
(1)3-甲基-2-丙基-1-戊烯结构简式为______________________。
(2) 名称为___________________________。
名称为___________________________。
(3) 名称为___________________________________。
名称为___________________________________。
(4)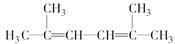 名称为___________________________。
名称为___________________________。
用系统命名法命名或写出结构简式:
(1)3-甲基-2-丙基-1-戊烯结构简式为______________________。
(2) 名称为___________________________。
名称为___________________________。
(3) 名称为___________________________________。
名称为___________________________________。
(4)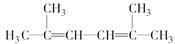 名称为___________________________。
名称为___________________________。