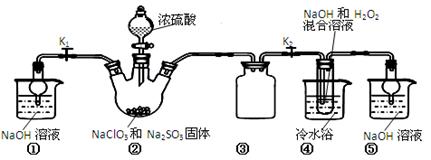
实验室采用如下图所示的装置,可将反应粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。
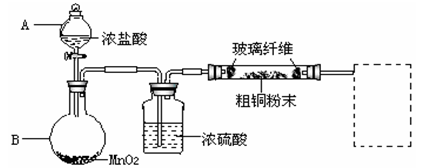
(1)仪器A的名称是 。
(2)连接好装置后,加入药品前,应该进行的实验操作是 。
(3)装置B中发生反应的离子方程式是 。
(4)有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”) 。
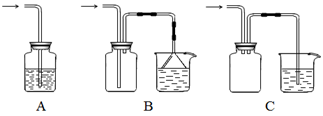
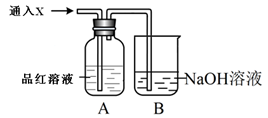
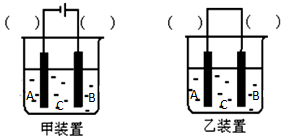
(5)虚线内缺少实验装置,请你画出装置图,标明药品名称。



 粤公网安备 44130202000953号
粤公网安备 44130202000953号