(1)在Cu+2H2SO4(浓)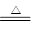 CuSO4+SO2↑+2H2O反应中,请用双线桥法标出元素化合价的升降、电子得失和被氧化、被还原的情况。
CuSO4+SO2↑+2H2O反应中,请用双线桥法标出元素化合价的升降、电子得失和被氧化、被还原的情况。
(2)维生素C能使食物中的Fe3+转化为Fe2+,即Fe3+ Fe2+
Fe2+
①在此变化中,Fe3+被_______(填氧化或还原,下同);维生素C是_______剂
②若有1molFe3+转化为Fe2+,则维生素C______(填得或失)_______mol电子
(1)在Cu+2H2SO4(浓)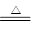 CuSO4+SO2↑+2H2O反应中,请用双线桥法标出元素化合价的升降、电子得失和被氧化、被还原的情况。
CuSO4+SO2↑+2H2O反应中,请用双线桥法标出元素化合价的升降、电子得失和被氧化、被还原的情况。
(2)维生素C能使食物中的Fe3+转化为Fe2+,即Fe3+ Fe2+
Fe2+
①在此变化中,Fe3+被_______(填氧化或还原,下同);维生素C是_______剂
②若有1molFe3+转化为Fe2+,则维生素C______(填得或失)_______mol电子