氯气是一种化学性质活泼的气体。
(1)新制备的氯水呈浅黄绿色,说明氯水中有 分子存在。向氯水中滴入几滴AgNO3溶液,现象是 。
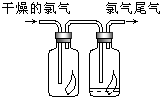
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察的现象是_ _
(3)为防止氯气污染空气,可用 溶液吸收多余的氯气,该反应的化学方程式为_____________
氯气是一种化学性质活泼的气体。
(1)新制备的氯水呈浅黄绿色,说明氯水中有 分子存在。向氯水中滴入几滴AgNO3溶液,现象是 。
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察的现象是_ _

(3)为防止氯气污染空气,可用 溶液吸收多余的氯气,该反应的化学方程式为_____________