(1)家用液化气的主要成分之一是丁烷(C4H10),当1kg丁烷完全燃烧生成二氧化碳和液态水时,放出热量为5×104kJ,试写出表示丁烷燃烧热的热化学方程式 。
(2)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热ΔH分别为-285.8 kJ/mol、-283.0 kJ/mol和-726.5 kJ/mol。请回答下列问题:
①用太阳能分解10 mol水消耗的能量是 kJ;
②甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式 ;
③研究NO2、SO2、CO等大气污染气体的处理具有重要意义,已知:
2SO2(g)+O2(g) = 2SO3(g) ΔH=-196.6 kJ/mol
2NO(g)+O2(g) = 2NO2(g) ΔH=-113.0 kJ/mol
则反应NO2(g)+SO2(g)=SO3(g)+NO(g)的ΔH= kJ/mol。
(3)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ•mol-1
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47.4kJ•mol-1
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ•mol-1
写出CO(g)还原FeO(s)得到Fe(s)体和CO2(g)的热化学反应方程式 .
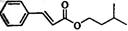 )是一种香料,一种合成路线如下:
)是一种香料,一种合成路线如下: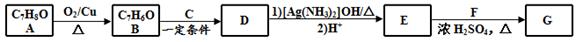
 ;
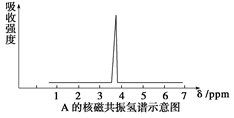
;
 粤公网安备 44130202000953号
粤公网安备 44130202000953号