粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(
、
、
).现以粗盐为原料制取精盐,生产过程如图所示
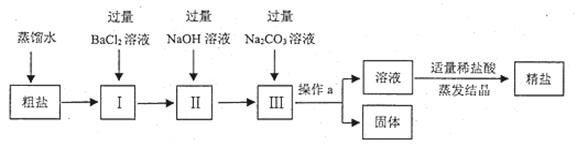
(1)写出I中发生反应的化学方程式。加入过量
溶液的目的是。
(2)操作a的名称是,该操作需要用到的玻璃仪器主要有:烧杯、、玻璃棒。
(3)加入适量稀盐酸的作用是除去溶液中的、(填化学式)。
(4)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是。
粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(
、
、
).现以粗盐为原料制取精盐,生产过程如图所示

(1)写出I中发生反应的化学方程式。加入过量
溶液的目的是。
(2)操作a的名称是,该操作需要用到的玻璃仪器主要有:烧杯、、玻璃棒。
(3)加入适量稀盐酸的作用是除去溶液中的、(填化学式)。
(4)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是。