碳酸钠和碳酸氢钠是生活中常见的盐,通过实验验证、探究它们的化学性质。
【查阅资料】
①Na2CO3 + CaCO3 = CaCO3↓+ 2NaCl
②2NaHCO3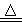 Na2CO3 +CO2↑+ H2O
Na2CO3 +CO2↑+ H2O
③Ca(HCO3)2易溶于水。
④CaCl2溶液分别与NaHCO3、Na2CO3溶液等体积混合现象(百分数为溶质质量分数)
| |
NaHCO3 |
Na2CO3 |
|||
| 0.1% |
1% |
5% |
0.1% |
||
| CaCl2 |
0.1% |
无明显现象 |
有浑浊 |
有浑浊 |
有浑浊 |
| 1% |
无明显现象 |
有浑浊 |
有浑浊,有微小气泡 |
有沉淀 |
|
| 5% |
无明显现象 |
有浑浊 |
有浑浊,有大量气泡 |
有沉淀 |
【进行实验】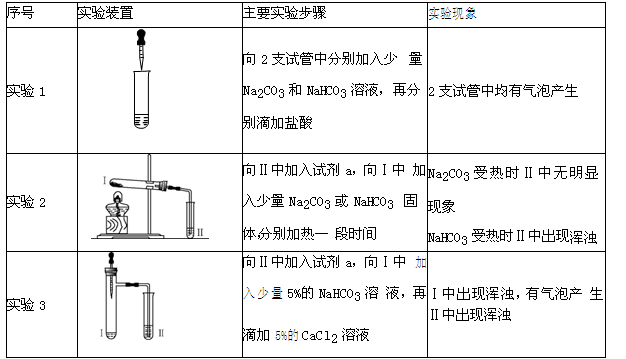
【解释与结论】
(1)实验1中,NaHCO3与盐酸反应的化学方程式为 。
(2)实验2中,试剂a为 。
(3)实验3中,NaHCO3与CaCl2反应的化学方程式为:
2NaHCO3+ CaCl2 ="=====" + + + H2O
【反思与评价】
(1)实验2中,加热NaHCO3后,试管Ⅰ中残留固体成分可能为 (写出所有可能)。
(2)资料④中,NaHCO3溶液与CaCl2溶液混合的现象中,有些只观察到浑浊、未观察到气泡,原因可能是 。



 粤公网安备 44130202000953号
粤公网安备 44130202000953号