【改编】(每空2分,共12分)下面A~F是几种常见烃的分子球棍模型。
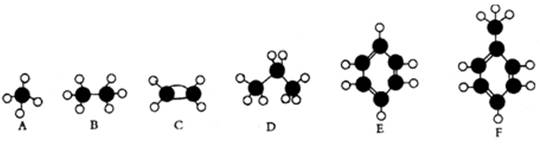
根据上述模型,回答下列问题:
(1)常温下含碳量最高的液态烃是 。
(2)能够发生加成反应的烃有 种。
(3)写出E与液溴在FeBr3催化下反应的方程式: ,反应类型:
(4)所有原子均在同一平面上的是 。
(5)能使酸性高锰酸钾溶液褪色的是 (填对应字母)。
【改编】(每空2分,共12分)下面A~F是几种常见烃的分子球棍模型。

根据上述模型,回答下列问题:
(1)常温下含碳量最高的液态烃是 。
(2)能够发生加成反应的烃有 种。
(3)写出E与液溴在FeBr3催化下反应的方程式: ,反应类型:
(4)所有原子均在同一平面上的是 。
(5)能使酸性高锰酸钾溶液褪色的是 (填对应字母)。