用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考下图,从下表中选出正确选项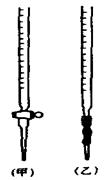
| |
锥形瓶中的溶液 |
滴定管中的溶液 |
选用指示剂 |
选用滴定管 |
| A |
碱 |
酸 |
石蕊 |
(乙) |
| B |
酸 |
碱 |
酚酞 |
(甲) |
| C |
碱 |
酸 |
甲基橙 |
(甲) |
| D |
酸 |
碱 |
石蕊 |
(乙) |
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考下图,从下表中选出正确选项
| |
锥形瓶中的溶液 |
滴定管中的溶液 |
选用指示剂 |
选用滴定管 |
| A |
碱 |
酸 |
石蕊 |
(乙) |
| B |
酸 |
碱 |
酚酞 |
(甲) |
| C |
碱 |
酸 |
甲基橙 |
(甲) |
| D |
酸 |
碱 |
石蕊 |
(乙) |