某工厂对工业生产钛白粉产生的废液进行综合利用,废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,可用于生产颜料铁红和补血剂乳酸亚铁。其生产工艺流程如下:(已知乳酸酸性强于碳酸)
已知:①TiOSO4可溶于水,在水中可以电离为TiO2+和SO42—;
②TiOSO4水解的反应为:TiOSO4+(x+1)H2O →TiO2 • xH2O↓+H2SO4。
请回答:
(1)步骤①所得滤渣的主要成分为 ,分离硫酸亚铁溶液和滤渣的操作中所用的玻璃仪器是 ;步骤②中得到纯净硫酸亚铁晶体的操作为蒸发浓缩、 。
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为 。
(3)步骤④的离子方程式是 。
(4)试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因: 。
(5)实验室中常用KMnO4滴定法测定晶体中FeSO4·7H2O的质量分数,取步骤②中所得FeSO4·7H2O晶体样品a g,配成500.00 mL溶液,取出25.00 mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000 mol•L-1 KMnO4溶液25.00 mL,所得晶体中FeSO4·7H2O的质量分数为(用a表示) 。
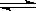 4NH3(g)+3O2(g) △H =" a" kJ.mol-1
4NH3(g)+3O2(g) △H =" a" kJ.mol-1 g)
g)  2N2(g) + 6H2O(l)
2N2(g) + 6H2O(l)  1mol·L-1的NaOH溶液的pH为11,则该温度下水的Kw= .
1mol·L-1的NaOH溶液的pH为11,则该温度下水的Kw= . 2C(g)+D(s),达到平衡时,C的浓度为0.4mol·L-1。
2C(g)+D(s),达到平衡时,C的浓度为0.4mol·L-1。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号