(8分)某学生设计了如下实验:
 |
回答下列问题:
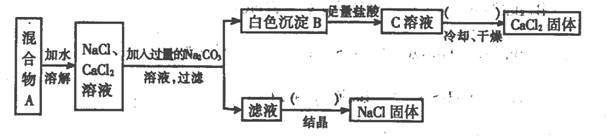
(1)该同学的实验目的是 ;
(2)上图括号内的操作均为 ;
(3)按此实验方案得到的NaCl固体中肯定含有 杂质(填化学式);为了解决这个问题可以向过滤得到的滤液中加入适量的 ;
(8分)某学生设计了如下实验:
 |
回答下列问题:
(1)该同学的实验目的是 ;
(2)上图括号内的操作均为 ;
(3)按此实验方案得到的NaCl固体中肯定含有 杂质(填化学式);为了解决这个问题可以向过滤得到的滤液中加入适量的 ;