X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)Y基态原子的电子排布式是 ;Z所在周期中第一电离能最大的元素是 。
(2)XY2- 离子的立体构型是 ;R2+的水合离子中,提供孤电子 对的原子是 。
(3)Z与某元素形成的化合物的晶胞如下图所示,晶胞中阴离子与阳离子的个数比是 。
(4)将R单质的粉末加入XH3的浓溶液中,通入Y2,充分反应后溶液呈深蓝色,该反应的离子方程式是 。
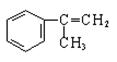
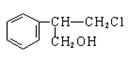

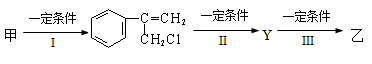
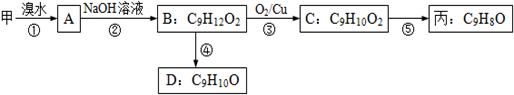
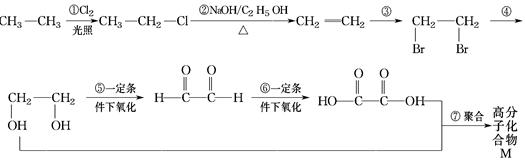
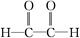 和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式
和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式 粤公网安备 44130202000953号
粤公网安备 44130202000953号