实验室用下列仪器组装一套蒸馏食盐水的装置,并进行蒸馏得到蒸馏水。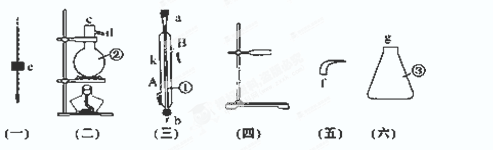
(1)、写出下列仪器的名称:①_____;②____;③______。
(2)、可用于分离或提纯物质的方法有
A 过滤 B 升华 C 加热分解 D.洗气法 E. 蒸馏 F.结晶 G.萃取 H.分液
下列各组混合物的分离或提纯应选用上述哪种方法最合适?(填字母)
① 分离乙醇与水的混合物,用 。
②从硝酸钾和氯化钾混合液中获取硝酸钾,用 。
实验室用下列仪器组装一套蒸馏食盐水的装置,并进行蒸馏得到蒸馏水。
(1)、写出下列仪器的名称:①_____;②____;③______。
(2)、可用于分离或提纯物质的方法有
A 过滤 B 升华 C 加热分解 D.洗气法 E. 蒸馏 F.结晶 G.萃取 H.分液
下列各组混合物的分离或提纯应选用上述哪种方法最合适?(填字母)
① 分离乙醇与水的混合物,用 。
②从硝酸钾和氯化钾混合液中获取硝酸钾,用 。