为确定某酸HA是弱电解质,两同学的实验方案如下:
甲:①称取一定质量的HA,配制0.1 mol·L-1的溶液100 mL;
②用pH计测出该溶液的pH,根据pH="-lg" c(H+),推算出溶液中H+的浓度,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制0.1mol·L-1的两种酸溶液各100 mL;
②分别取配制的这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是___ ___。
(2)甲方案中说明HA是弱电解质的理由是测得溶液的H+的浓度_ _0.1 mol·L-1(选填“>”、“<”或“=”)。
(3)乙方案中说明HA是弱电解质的现象是_ __。
A.装盐酸的试管中放出气体的速率快;
B.装HA溶液的试管中放出气体的速率快;
C.两个试管中产生气体的速率一样快。
(4)请你评价:乙方案中的不妥之处:______ ___________________________。
(5)已知在T°C时,0.1 mol·L-1HA溶液中HA的电离度为5%,求该温度下HA的电离常数(写出计算过程)
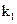 、
、 ,打开
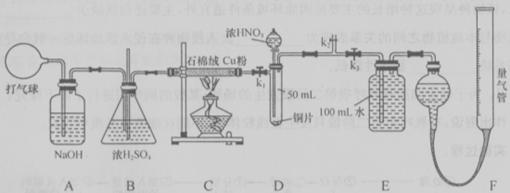
,打开 ,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入
,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入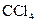 至满。则D中一定发生反应的离子方程式为:_________;
至满。则D中一定发生反应的离子方程式为:_________;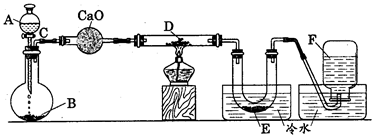
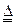 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。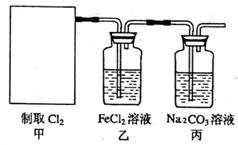
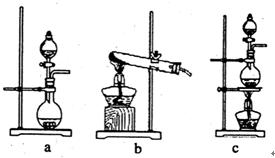
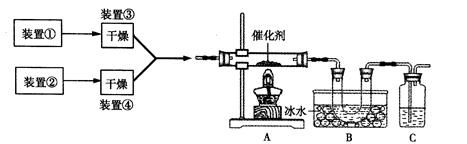
 制得纯净干燥的SO3,若C中盛放NaOH溶液,则此装置中存在明显不足,应如何改进(从下面给出的实验装置中选择字母标号补充或替换,并用简要文字说明)
制得纯净干燥的SO3,若C中盛放NaOH溶液,则此装置中存在明显不足,应如何改进(从下面给出的实验装置中选择字母标号补充或替换,并用简要文字说明)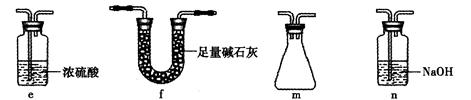

 可)
可) 粤公网安备 44130202000953号
粤公网安备 44130202000953号