(1)0.3 mol NH3分子中所含氢原子数与 个H2O分子中所含氢原子数相等。
(2)含0.4 mol Al3+的Al2(SO4)3中所含的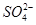 物质的量是 。
物质的量是 。
(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为 。
(4)2.3 g Na是 mol,含 mol e-。
(5)如果ag某气体中含有的分子数为b,则cg该气体的物质的量是(设NA为阿伏加德罗常数) mol。
(1)0.3 mol NH3分子中所含氢原子数与 个H2O分子中所含氢原子数相等。
(2)含0.4 mol Al3+的Al2(SO4)3中所含的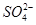 物质的量是 。
物质的量是 。
(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为 。
(4)2.3 g Na是 mol,含 mol e-。
(5)如果ag某气体中含有的分子数为b,则cg该气体的物质的量是(设NA为阿伏加德罗常数) mol。