某有机物A的结构简式为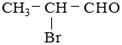 ,请回答下列问题。
,请回答下列问题。
(1)A中所含官能团的名称是 、 ;
(2)A可能发生的反应有 (填序号);
① 取代反应 ② 消去反应 ③ 水解反应 ④ 酯化反应
(3)将A与氢氧化钠的乙醇溶液混合并加热,再让得到的主要产物发生加聚反应,生成了某聚合物,该聚合物的结构简式是 。
某有机物A的结构简式为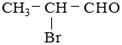 ,请回答下列问题。
,请回答下列问题。
(1)A中所含官能团的名称是 、 ;
(2)A可能发生的反应有 (填序号);
① 取代反应 ② 消去反应 ③ 水解反应 ④ 酯化反应
(3)将A与氢氧化钠的乙醇溶液混合并加热,再让得到的主要产物发生加聚反应,生成了某聚合物,该聚合物的结构简式是 。