醛可以发生分子间反应,生成羟基醛。如: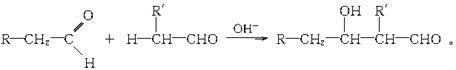 烯烃分子则在一定条件下会发生二分子聚合。如: CH2—CH==CH2
烯烃分子则在一定条件下会发生二分子聚合。如: CH2—CH==CH2
 。
。
(1)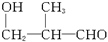 可由_________与______________两种醛合成。(填结构简式)
可由_________与______________两种醛合成。(填结构简式)
(2) 转变为
转变为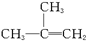 须依次经过__________、__________和_____________等较合理的反应过程。(填反应类型)
须依次经过__________、__________和_____________等较合理的反应过程。(填反应类型)
(3)将 经两分子聚合后的生成物与氢气加成,所得产物按系统命名法称作__________________。
经两分子聚合后的生成物与氢气加成,所得产物按系统命名法称作__________________。
醛可以发生分子间反应,生成羟基醛。如: 烯烃分子则在一定条件下会发生二分子聚合。如: CH2—CH==CH2
烯烃分子则在一定条件下会发生二分子聚合。如: CH2—CH==CH2
 。
。
(1)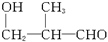 可由_________与______________两种醛合成。(填结构简式)
可由_________与______________两种醛合成。(填结构简式)
(2) 转变为
转变为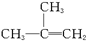 须依次经过__________、__________和_____________等较合理的反应过程。(填反应类型)
须依次经过__________、__________和_____________等较合理的反应过程。(填反应类型)
(3)将 经两分子聚合后的生成物与氢气加成,所得产物按系统命名法称作__________________。
经两分子聚合后的生成物与氢气加成,所得产物按系统命名法称作__________________。