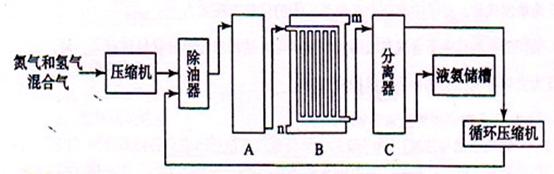
能源问题日益成为制约世界经济发展的瓶颈,开发新能源,寻找经济发展的新动力,已受到许多国家的高度重视。二甲醚(CH3OCH3)可能成为未来替代柴油和液化气的洁净液体燃料,工业上在一定条件下以CO和H2为原料生产二甲醚的新工艺主要发生三个反应:
| 编号 |
热化学方程式 |
化学平衡常数 |
| ① |
CO(g)+2H2(g) CH3OH(g) △H1=-91kJ·mol-1 CH3OH(g) △H1=-91kJ·mol-1 |
K1 |
| ② |
2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-24kJ·mol-1 CH3OCH3(g)+H2O(g) △H2=-24kJ·mol-1 |
K2 |
| ③ |
CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41kJ·mol-1 CO2(g)+H2(g) △H3=-41kJ·mol-1 |
K3 |
回答下列问题:
(1)新工艺的总反应为:3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) △H
CH3OCH3(g)+CO2(g) △H
该反应△H= ,化学平衡常数K= (用含K1、K2、K3的代数式表示)。
(2)下列措施中,能提高CH3OCH3产率的有 。
A 使用过量的CO B 升高温度 C 增大压强
D 通入水蒸气 E.改用高效催化剂
(3)原工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生。新工艺中反应③的发生提高了CH3OCH3的产率,原因是 。
(4)为了寻找合适的反应温度,研究者进行了一系列试验,则每次试验应保持 等因素不变。试验结果如下图,CO转化率随温度变化的原因是 。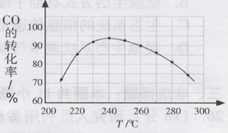




 CO2 (g)+ H2 (g),已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于
CO2 (g)+ H2 (g),已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于  CO(g)+H2(g) , 试分析和回答下列问题:
CO(g)+H2(g) , 试分析和回答下列问题: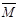 的取值范围是。
的取值范围是。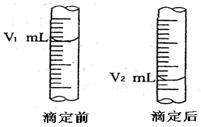
 粤公网安备 44130202000953号
粤公网安备 44130202000953号