(12分)反应N2(g)+3H2(g) 2NH3(g) △H<0,在等容条件下进行。改变其它反应条件,在I、II、III阶段体系中c(H2)和c(NH3)随时间变化的曲线如下图所示:
2NH3(g) △H<0,在等容条件下进行。改变其它反应条件,在I、II、III阶段体系中c(H2)和c(NH3)随时间变化的曲线如下图所示: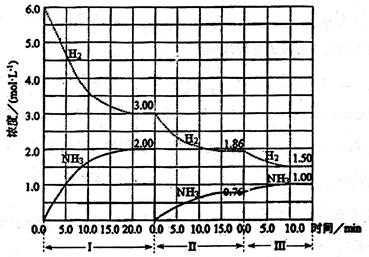
请回答下列问题:
(1)N2的平均反应速率vI(N2)、vII(N2)、vIII(N2)从大到小排列次序为 。
(2)比较第II阶段反应温度(T2)和第III阶段反应温度(T3)的高低:T2 T3(填“>”、“=”或“<”),判断的理由是 。
(3)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示IV阶段体系中c(H2)和c(NH3)随时间变化的曲线(曲线上必须标出具体物质)。
(4)资料提示:
①将氨气通入双氧水中可发生反应:3H2O2+2NH3=N2+6H2O △H<0,此反应可设计成原电池。
②用如图所示装置电解尿素[CO(NH2)2]的碱性溶液可以制取N2、H2(注:电解池中隔膜仅阻止气体通过)。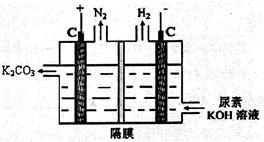
上述原电池的正极反应式为 ;
上述电解池的阳极反应式为 。
相关知识点
 2SO3(g),反应过程的能量变化如下图所示。已知1mol SO2(g)氧化为1 mol SO3(g)的△H="–99" kJ/mol。请回答下列问题:
2SO3(g),反应过程的能量变化如下图所示。已知1mol SO2(g)氧化为1 mol SO3(g)的△H="–99" kJ/mol。请回答下列问题:
 2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
2NO(g) DH=a kJ·mol-1的平衡常数K如下表: pC达到平衡,若:
pC达到平衡,若: ;将C催化加氢生成环戊烷。试写出A、B、C的结构简式。
;将C催化加氢生成环戊烷。试写出A、B、C的结构简式。 粤公网安备 44130202000953号
粤公网安备 44130202000953号