(18分)(1)原子结构与元素周期表存在着内在联系。根据所学物质结构知识,请你回答下列
问题:
①具有(n-1)d10ns2电子构型的元素位于周期表中________区和________族。
②日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素,该元素基态原子未成对电
子数为__________________。
(2)等电子原理——原子总数相同、价电子总数相同的粒子具有相似的化学键特征,它们的
许多性质是相近的。写出两种由多个原子组成的含有与N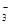 电子数相同的粒子的化学式
电子数相同的粒子的化学式
__________、____________。
(3)氯化亚砜(SOCl2)是一种很重要的化学试剂,可以作为氯化剂和脱水剂。氯化亚砜分子的
几何构型是______________;中心原子采取________杂化方式。
(4)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危
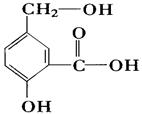
害人们健康。苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ 4种类型,苏丹红Ⅰ号的分子结构如图1所示。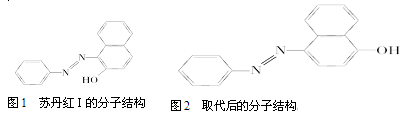
苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,
则其在水中的溶解度会______(填“增大”或“减小”),原因是____________________。
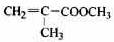
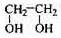


 ) (丁)
) (丁)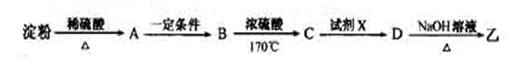
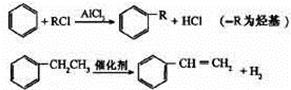
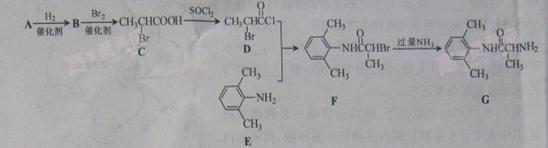
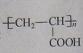 的单体,则A中含有的官能团是(写名称)。B的结构简式是。
的单体,则A中含有的官能团是(写名称)。B的结构简式是。 b.能使酸性高锰酸钾溶液褪色
b.能使酸性高锰酸钾溶液褪色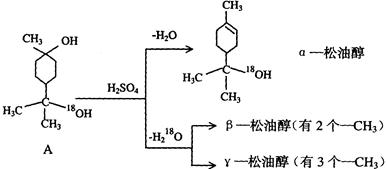
 α-松油醇的分子式;
α-松油醇的分子式;

 粤公网安备 44130202000953号
粤公网安备 44130202000953号