在某有机物A的分子的结构简式如右图。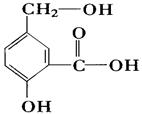
(1) A中具有 、 官能团
(写官能团名称)
(2)A跟NaOH溶液反应的化学方程式是
(3)A跟NaHCO3溶液反应的化学方程式是
(4)A在一定条件下与乙醇反应的化学方程式是

在某有机物A的分子的结构简式如右图。
(1) A中具有 、 官能团
(写官能团名称)
(2)A跟NaOH溶液反应的化学方程式是
(3)A跟NaHCO3溶液反应的化学方程式是
(4)A在一定条件下与乙醇反应的化学方程式是
