研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
()+()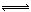 ()+() ∆(I)
()+() ∆(I)
()+()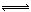 () ∆(II)
() ∆(II)
(1)()+()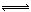 ()+()+()的平衡常数= (用、表示)。
()+()+()的平衡常数= (用、表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向恒容密闭容器中加入 和 ,时反应(II)达到平衡。测得内()=×-•L-•-,则平衡后n()= ,的转化率= 。其它条件保持不变,反应(II)在恒压条件下进行,平衡时的转化率(填""""或""),平衡常数(填"增大""减小"或"不变"。若要使减小,可采用的措施是 。
(3)实验室可用溶液吸收,反应为+2NaOH=++。含 NaOH的水溶液与 恰好完全反应得溶液A,溶液B为•‾1的溶液,则两溶液中c(‾)、c(-)和c(‾)由大到小的顺序为。(已知的电离常数=×-•L‾,的电离常数=×-•‾,可使溶液A和溶液B的相等的方法是 () 。
| A. |
a.向溶液A中加适量水 b.向溶液A中加适量c.向溶液B中加适量水 d.向溶液B中加适量 |
相关知识点
 所示转化关系,D的分子式为
所示转化关系,D的分子式为
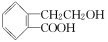 ,它可通过不同化学反应分别制得B、C和D三种物质。
,它可通过不同化学反应分别制得B、C和D三种物质。
 Li的质量是g。
Li的质量是g。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号