A、B、C、D、E、F为原子序数依次增大的短周期元素,B、C相邻且同周期,A、D同主族。C原子最外层电子数是核外电子层数的3倍,A、C能形成两种化合物甲和乙,原子个数比分别为2∶1和1∶1,甲为常见的溶剂。E是地壳中含量最多的金属元素;F元素为同周期电负性最大的元素。D和F可形成化合物丙,E和F可形成化合物丁。G为第四周期未成对电子数最多的元素。请回答下列问题:
(1)写出G基态原子的价电子排布式 。
(2) B和C比较,第一电离能较大的是 (填元素符号),其原因为 。
(3)甲、乙两分子的中心原子的杂化类型是否相同 (相同、不相同)。
(4)已知化合物丁熔点190℃,沸点183℃。丙和丁比较,熔点较高的是 (填化学式),
(5)配合物戊由G3+与甲、元素F构成,已知该配合物的配位数为6。在含有0.1mol戊的溶液中加入AgNO3溶液至过量,经过滤、洗涤、干燥后,得到28.7g白色沉淀。,则戊的化学式为 。
 ____________ 、_______________________、________________________。
____________ 、_______________________、________________________。
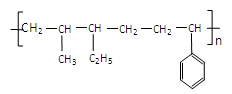 结构的橡胶。
结构的橡胶。 _____
_____ 乙偶姻中只含有C、H、O三种元素,其相对分子质量为88,分子中C、H、O原子个数比为2:4:1 。
乙偶姻中只含有C、H、O三种元素,其相对分子质量为88,分子中C、H、O原子个数比为2:4:1 。
 式是______________。
式是______________。 _____;
_____; ;
;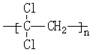 )具有超强阻隔性能,可作为保鲜食品的包装材料。它是由____________________(写结构简式)发生加聚反应生成的。
)具有超强阻隔性能,可作为保鲜食品的包装材料。它是由____________________(写结构简式)发生加聚反应生成的。 H(CH2)7COOH]含量很低。下列关于亚油酸的说法中,正确的是____________________________(填序号)。
H(CH2)7COOH]含量很低。下列关于亚油酸的说法中,正确的是____________________________(填序号)。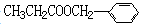 )在食品、药品、化妆品等方面应用广泛,用烷烃A合成香精及其它两种有机物的路线如下。
)在食品、药品、化妆品等方面应用广泛,用烷烃A合成香精及其它两种有机物的路线如下。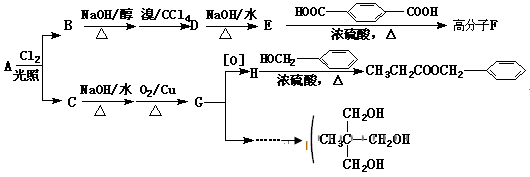
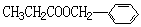 互为同分异构体的是____________________ (填序号)。
互为同分异构体的是____________________ (填序号)。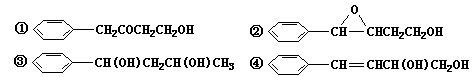
 ___________________;
___________________;


 既能起银镜反应,遇FeCl3溶液又能呈紫色的同分异构体的结构简式 。
既能起银镜反应,遇FeCl3溶液又能呈紫色的同分异构体的结构简式 。 粤公网安备 44130202000953号
粤公网安备 44130202000953号