(1)将等物质的量的KI和CuCl2溶于水,用惰性电极电解,该电解反应可分为________个阶段(表格不一定填满,若不够还可以自行添加)。
| 阶段 |
相当于电解什么溶液 |
离子方程式 |
| ① |
|
|
| ② |
|
|
| ③ |
|
|
| ④ |
|
|
| ⑤ |
|
|
(2)画出过程中溶液pH随时间变化的曲线(假定生成的Cl2全部逸出)。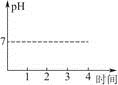
(1)将等物质的量的KI和CuCl2溶于水,用惰性电极电解,该电解反应可分为________个阶段(表格不一定填满,若不够还可以自行添加)。
| 阶段 |
相当于电解什么溶液 |
离子方程式 |
| ① |
|
|
| ② |
|
|
| ③ |
|
|
| ④ |
|
|
| ⑤ |
|
|
(2)画出过程中溶液pH随时间变化的曲线(假定生成的Cl2全部逸出)。