(1)钒触媒(V2O5)能加快SO2的氧化速率,此过程中SO2先与V2O5反应生成V2O4。该过程的化学方程式可表示为__________________________________________。
(2)为测定过程中混合气的SO2体积分数,选用0.0500 mol/L I2的标准溶液、淀粉溶液进行测定。已知:V(耗用I2标准溶液)="10.00" mL,V(采集烟气)="100.0" mL(已折算为标准状况),则烟气中SO2 的体积分数为_____________________。
(3)一定温度时,SO2的平衡转化率(α)与体系总压强(p)的关系如图9所示。试分析工业生产中采用常压的原因是____________________。
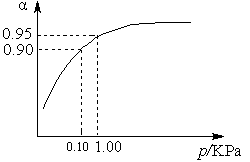
图9
(4)在温度相同、体积均为1 L的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。
已知:2SO2(g)+O2(g) 2SO3(g) ΔH ="-98.3" kJ·mol-1。
2SO3(g) ΔH ="-98.3" kJ·mol-1。
容 器
|
甲
|
乙
|
丙
|
反应物投入量
|
2 mol SO2、1 mol O2
|
2 mol SO3
|
m mol SO2、n mol O2、
p mol SO3
|
c(SO3) /mol·L-1
|
1.4
|
1.4
|
1.4
|
能量变化
|
放出a kJ
|
吸收b kJ
|
吸收c kJ
|
SO2或SO3的转化率
|
α1
|
α2
|
12.5%
|
则:α1+α2=_________________,p=________________mol,b+c=_______________kJ。